题目内容
 密闭容器中发生下列反应:N2+3H2?2NH3△H<0,如图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题:
密闭容器中发生下列反应:N2+3H2?2NH3△H<0,如图是某一时间段中反应速率与反应进程的曲线关系图.回答下列问题:(1)处于平衡状态的时间段是
(2)t1、t3、t4时刻,体系中分别是什么条件发生了变化?t1 时刻
(3)下列时间段中,氨的百分含量的大小关系是:t0-t1 t2-t3(填“>”“<”“=”)
(4)t6时刻,若升高温度,反应速率变化情况画在下图中.
考点:化学平衡建立的过程,化学反应速率的影响因素
专题:
分析:(1)根据平衡时正逆反应速率相等作判断;
(2)根据图可知,t1 时刻逆反应速率增大,正反应速率不变,所以可以判断是恒容条件下增加了生成物氨气;t3时刻正逆反应速率都同等程度的变大,平衡不移动,所以可以推断是使用了催化剂; t4时刻正逆反应速率都减小,且逆反应速率大于正反应速率,平衡逆向移动,所以可以推断是降低压强;
(3)t0-t1 和t2-t3这两个时间段相比,由于在t1 时刻增加了氨气,体系压强增大,所以t2-t3这个时间段氨气的百分含量高,据此答题;
(4)由于该反应是放热反应,升高温度正逆反应速率都会增大,平衡逆向移动,据此可画出图;
(2)根据图可知,t1 时刻逆反应速率增大,正反应速率不变,所以可以判断是恒容条件下增加了生成物氨气;t3时刻正逆反应速率都同等程度的变大,平衡不移动,所以可以推断是使用了催化剂; t4时刻正逆反应速率都减小,且逆反应速率大于正反应速率,平衡逆向移动,所以可以推断是降低压强;
(3)t0-t1 和t2-t3这两个时间段相比,由于在t1 时刻增加了氨气,体系压强增大,所以t2-t3这个时间段氨气的百分含量高,据此答题;
(4)由于该反应是放热反应,升高温度正逆反应速率都会增大,平衡逆向移动,据此可画出图;
解答:
解:(1)根据平衡时正逆反应速率相等可知,在图中t0-t1 、t2-t4、t5-t6反应都处于平衡状态,故答案为:t0-t1 、t2-t4、t5-t6;
(2)根据图可知,t1 时刻逆反应速率增大,正反应速率不变,所以可以判断是恒容条件下增加了生成物氨气;t3时刻正逆反应速率都同等程度的变大,平衡不移动,所以可以推断是使用了催化剂; t4时刻正逆反应速率都减小,且逆反应速率大于正反应速率,平衡逆向移动,所以可以推断是降低压强,故答案为:恒容条件下,充入氨气;加催化剂;降低压强;
(3)t0-t1 和t2-t3这两个时间段相比,由于在t1 时刻增加了氨气,体系压强增大,所以t2-t3这个时间段氨气的百分含量高,故答案为:<;
(4)由于该反应是放热反应,升高温度正逆反应速率都会增大,平衡逆向移动,据此可画出图为: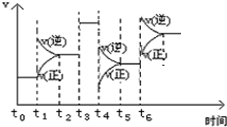 ,故答案为:
,故答案为: ;
;
(2)根据图可知,t1 时刻逆反应速率增大,正反应速率不变,所以可以判断是恒容条件下增加了生成物氨气;t3时刻正逆反应速率都同等程度的变大,平衡不移动,所以可以推断是使用了催化剂; t4时刻正逆反应速率都减小,且逆反应速率大于正反应速率,平衡逆向移动,所以可以推断是降低压强,故答案为:恒容条件下,充入氨气;加催化剂;降低压强;
(3)t0-t1 和t2-t3这两个时间段相比,由于在t1 时刻增加了氨气,体系压强增大,所以t2-t3这个时间段氨气的百分含量高,故答案为:<;
(4)由于该反应是放热反应,升高温度正逆反应速率都会增大,平衡逆向移动,据此可画出图为:
 ,故答案为:
,故答案为: ;
;
点评:本题主要考查了化学平衡的特征及影响平衡移动的外界因素、用图示表示平衡移动的情况等知识点,中等难度,解题的关键在于正确理解时间-速率图.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
 如图表示可逆反应:N2(g)+3H2(g)═2NH3(g)达到化学平衡状态时外界条件影响导致平衡移动的曲线,根据判断影响平衡移动的因素是( )
如图表示可逆反应:N2(g)+3H2(g)═2NH3(g)达到化学平衡状态时外界条件影响导致平衡移动的曲线,根据判断影响平衡移动的因素是( )| A、升高温度,同时加压 |
| B、减小压强,同时降温 |
| C、增大反应物的浓度,使用催化剂 |
| D、增大反应物的浓度,同时减小生成物的浓度 |
有机物中的烃是 ( )的化合物.
| A、含有碳元素 |
| B、含有碳元素和氢元素 |
| C、仅含有碳元素和氢元素 |
| D、燃烧后生成二氧化碳和水 |
下列物质中,能使铁溶解,又不能生成沉淀和气体的是( )
| A、稀H2SO4 |
| B、浓H2SO4 |
| C、AgNO3溶液 |
| D、Fe2(SO4)3 |
 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表: