题目内容
将铜粉放入稀硫酸中,加热无明显现象发生.但加入某盐后,发现铜粉质量逐渐减少,则该盐可能是( )
| A、Fe2(SO4)3 |
| B、ZnSO4 |
| C、KNO3 |
| D、NaCl |
考点:铜金属及其重要化合物的主要性质
专题:几种重要的金属及其化合物
分析:铜粉与稀硫酸不反应,可以与稀硝酸反应,原来溶液中存在氢离子,有硝酸根离子存在时具有强氧化性,此外铜还可以和三价铁反应.
解答:
解:A、金属铜可以和三价铁离子之间反应生成铜离子和亚铁离子,故A选;
B、金属铜和稀硫酸不反应,加入硫酸锌也不反应,故B不选;
C、加入硝酸钾在酸性条件下,有很强的氧化性,能和金属铜之间反应,发生反应的离子方程式应该是:8H++2NO3-+3Cu=3Cu2++4H2O+2NO↑,故C选;
D、金属铜和稀盐酸、稀硫酸之间均不反应,所以加入氯化钠,不发生反应,故D不选;
故选AC.
B、金属铜和稀硫酸不反应,加入硫酸锌也不反应,故B不选;
C、加入硝酸钾在酸性条件下,有很强的氧化性,能和金属铜之间反应,发生反应的离子方程式应该是:8H++2NO3-+3Cu=3Cu2++4H2O+2NO↑,故C选;
D、金属铜和稀盐酸、稀硫酸之间均不反应,所以加入氯化钠,不发生反应,故D不选;
故选AC.
点评:铜粉与稀硝酸可以反应,可以直接加入硝酸,也可以先加盐酸或硫酸,再加入硝酸盐,其作用是一样的.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
以下基态原子的电子排布式不符合构造原理的是( )
| A、1s22s22p63s23p63d74s2 |
| B、1s22s22p63s23p63d54s1 |
| C、1s22s22p63s23p63d104s24p1 |
| D、1s22s22p63s23p64s2 |
下列有关实验操作或装置正确的是( )


| A、用图1所示装置进行乙酸乙酯水解 |
| B、用图2所示装置实验室制取乙烯 |
| C、碘水用CCl4萃取分液后再蒸馏,可得到I2 |
| D、梨形分液漏斗检漏,加水后玻璃旋塞处是否漏水即可 |
核电荷数小于或等于18的元素中,原子的最外层电子数是其余电子总数一半的元素种类有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
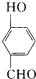 比
比 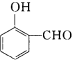 的沸点
的沸点