题目内容
将一含有杂质的铁粉10g 投入足量100g稀盐酸中(杂质不与盐酸反应)反应后过滤得滤液质量为105.4g,求铁粉中铁的质量分数.
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:Fe+2HCl=FeCl2+H2↑,计算溶液质量增重,再根据方程式计算Fe的质量,进而计算Fe的质量分数.
解答:
解:设铁粉中Fe的质量为m,则:
Fe+2HCl=FeCl2+H2↑ 溶液质量增重
56 54
m 105.4g-100g=5.4g
故m=
=5.6g
故铁粉中Fe的质量分数为
×100%=56%,
答:铁粉中铁的质量分数为56%.
Fe+2HCl=FeCl2+H2↑ 溶液质量增重
56 54
m 105.4g-100g=5.4g
故m=
| 56×5.4g |
| 54 |
故铁粉中Fe的质量分数为
| 5.6g |
| 10g |
答:铁粉中铁的质量分数为56%.
点评:本题考查化学方程式的有关计算,利用差量法计算避免常规方法的繁琐,难度不大.

练习册系列答案
相关题目
以下物质可能是天然蛋白质水解产物的是( )
A、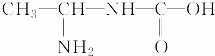 |
B、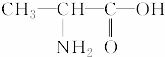 |
| C、CH3CH2COOH |
| D、CH3CH2CH2OH |
某有机物是药物生产的中间体,其结构如图.下列有关叙述不正确的是( )
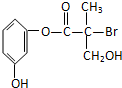

| A、该有机物与浓溴水可发生取代反应,1 mol该有机物可消耗3 mol溴 |
| B、该有机物与浓硫酸混合共热可发生消去反应 |
| C、1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH |
| D、1 mol该有机物催化加氢最多消耗3 mol氢气 |
“碳捕捉和储存(CCS)技术”是指通过碳捕捉技术,将工业和有关能源产业所产生的二氧化碳分离出来再利用,能降低二氧化碳等温室气体的排放,是当前科学家研究的重要课题.下列有关说法正确的是( )
| A、人类应将大气中的二氧化碳全部捕捉,以防产生温室效应 |
| B、用过氧化钠吸收CO2是目前比较经济的减碳方案 |
| C、16O=C=18O与16O=C=16O互为同位素且化学性质相似 |
| D、以捕捉到的二氧化碳为原料,用来制备甲醇等产品 |
下列叙述正确的是( )
| A、晶体中只要有阳离子就一定有阴离子 |
| B、金刚石和冰在熔化时克服的作用力相同 |
| C、HCl晶体由H+和Cl-构成 |
| D、原子晶体里,所有原子都以共价键相互结合 |
下列化学用语表示正确的是( )
| A、Na+的电子排布式:1s22s22p63s1 |
| B、Fe的简化电子排布式:[Ar]4s2 |
| C、Cr的外围电子排布式:3d54s1 |
D、N的最外层电子排布图: |
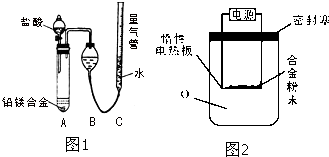 为测定某含铝95%一97%的铝镁合金(不含其它元素)中铝的质量分数,研究性学习小组的三位同学分别设计下列三种不同实验方案进行探究.填写下列空白.
为测定某含铝95%一97%的铝镁合金(不含其它元素)中铝的质量分数,研究性学习小组的三位同学分别设计下列三种不同实验方案进行探究.填写下列空白. 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: