题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1L 1mol?L-1的NaClO溶液中含ClO-的数目为NA |
| B、78 g 苯含有碳碳双键的数目为3NA |
| C、12.0g熔融的NaHSO4 中含有的阳离子数为0.2NA |
| D、乙烯和乙醇共1 mol,完全燃烧消耗O2的分子数为3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、ClO-是弱酸根,在溶液中会水解;
B、苯不是单双键交替的结构;
C、NaHSO4在熔融状态下只能电离出Na+和HSO4-;
D、1mol乙烯和1mol乙醇消耗的氧气的物质的量相同.
B、苯不是单双键交替的结构;
C、NaHSO4在熔融状态下只能电离出Na+和HSO4-;
D、1mol乙烯和1mol乙醇消耗的氧气的物质的量相同.
解答:
解:A、ClO-是弱酸根,在溶液中会水解,故ClO-的个数小于NA,故A错误;
B、苯不是单双键交替的结构,故B错误;
C、NaHSO4在熔融状态下只能电离出Na+和HSO4-,12g熔融的NaHSO4 的物质的量为0.1mol,故电离出的阳离子的物质的量为0.1mol,故C错误;
D、1mol乙烯和1mol乙醇消耗的氧气的物质的量相同,均为3mol,故乙烯和乙醇共1 mol,完全燃烧消耗O2的分子数为3NA,故D正确.
故选D.
B、苯不是单双键交替的结构,故B错误;
C、NaHSO4在熔融状态下只能电离出Na+和HSO4-,12g熔融的NaHSO4 的物质的量为0.1mol,故电离出的阳离子的物质的量为0.1mol,故C错误;
D、1mol乙烯和1mol乙醇消耗的氧气的物质的量相同,均为3mol,故乙烯和乙醇共1 mol,完全燃烧消耗O2的分子数为3NA,故D正确.
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、敞口久置的氯水中滴入石蕊试液,溶液先变红后褪色 |
| B、欲除去Cl2中少量的HCl气体,可将此混合气体通过盛有饱和食盐水的洗气瓶 |
| C、漂白粉的有效成分是Ca(ClO)2和CaCl2,应密封保存 |
| D、实验室用MnO2和稀HCl加热制Cl2,若有14.6g HCl参加反应,可得Cl2 3.55g |
下列关于太阳能、生物质能、氢能的说法不正确的是( )
| A、太阳能是地球上最基本的能源,绿色植物通过光合作用将太阳能转化成化学能 |
| B、农业上的秸秆、枝叶、水生植物、动物粪便及城市和工业的有机废弃物(如废弃塑料、橡胶等)都蕴藏着丰富的生物质能 |
| C、生物质能的利用主要有直接燃烧、生物化学转化、热化学转化等形式 |
| D、氢能是理想的清洁能源,但氢气的获取、贮存、运输等一直阻碍着人们大量利用氢能的步伐;贮氢合金的发现和利用,开辟了解决氢气贮存、运输难题的新途径 |
下列关于原子的说法中,正确的是( )
| A、原子不能再分 |
| B、原子是构成物质的一种微粒 |
| C、原子核都是由质子和中子构成的 |
| D、原子不显电性是由于原子是由一些不带电的微粒的构成的 |
下列化学用语书写正确的是( )
A、氯原子的结构示意图: | ||||||||
B、用电子式表示氯化氢分子的形成过程:H?:
| ||||||||
C、氯化镁的电子式: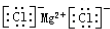 | ||||||||
| D、甲烷的结构式:CH4 |
有机物A含有C、H、O三种元素.A分子中含有一个羧基,且含碳40.0%、含氢约6.67%.将0.90gA配成100 mL溶液,取此溶液20.00 mL,用0.10 mol/LNaOH溶液滴定,至滴定终点时,消耗NaOH溶液20.00 mL.对有机物A的分析结论错误的是( )
| A、A的最简式为CH2O |
| B、A可以发生氧化反应,不能发生还原反应 |
| C、A的同分异构体中可能含有二元醛 |
| D、若A为羟基酸时,能生成六元或八元环状内酯 |
下列化学用语正确的是( )
A、乙烯(电子式为H:
| ||||||||
B、CO2的球棍模型: | ||||||||
C、氯化镁的电子式: | ||||||||
D、K+的结构示意图: |