题目内容
4.选用正确的实验操作,将下列各组物质进行分离或提纯.A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(1)分离CCl4和H2O:A (填字母,下同).
(2)除去石灰水中的CaCO3:B.
(3)除去CaO固体中少量的CaCO3固体:F.
(4)从碘水中提取碘:C.
(5)分离乙醇(沸点为78℃)和甲苯(沸点为110.6℃)的液体混合物:D.
分析 (1)CCl4和H2O分层;
(2)CaCO3不溶于水;
(3)CaCO3固体高温分解生成CaO;
(4)碘不易溶于水,易溶于有机溶剂;
(5)乙醇(沸点为78℃)和甲苯(沸点为110.6℃)互溶,但沸点不同.
解答 解:(1)CCl4和H2O分层,选择分液法分离,故答案为:A;
(2)CaCO3不溶于水,选择过滤法分离,故答案为:B;
(3)CaCO3固体高温分解生成CaO,选择高温分解法除杂,故答案为:F;
(4)碘不易溶于水,易溶于有机溶剂,选择萃取分液法分离,故答案为:C;
(5)乙醇(沸点为78℃)和甲苯(沸点为110.6℃)互溶,但沸点不同,选择蒸馏法分离,故答案为:D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离方法、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
相关题目
10.用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 用铁做两电极电解饱和食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标准状况下) | |
| B. | 标准状况下,2.24LHF中含有的原子数为0.2NA | |
| C. | 78g由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA | |
| D. | 在浓硫酸作用下,60g冰醋酸与足量无水乙醇反应生成乙酸乙酯的分子数为NA |
15.某反应由两步反应构成,反应过程中的能量变化曲线如图,下列叙述正确的是( )
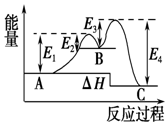

| A. | 两步反应均为吸热反应 | B. | 整个反应的△H=E1-E2+E3-E4 | ||
| C. | 整个反应的△H=E1-E2 | D. | 三种化合物中B最稳定 |
12.下列说法正确的是( )
| A. | NA 约等于6.02×1023 | |
| B. | 标准状况下气体摩尔体积约为22.4L | |
| C. | 1mol氧气的质量为16g | |
| D. | 在同温同压下,相同体积的任何气体单质所含分子数相同 |
19.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | SO2、SiO2、CO、P2O5都是非金属元素形成的氧化物,均为酸性氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | 有色玻璃、稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| D. | HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
9.某同学用托盘天平称量镁粉25.6g(1g以下用游码),他把镁粉放在左盘,当天平平衡时,所称取的镁粉的实际质量是( )
| A. | 25.6g | B. | 24.4g | C. | 24.6g | D. | 262g |
16.在标准状况下,a g气体X与b g气体Y的分子数相同,下列说法正确的是( )
| A. | 标准状况下,等质量的X和Y体积之比为a:b | |
| B. | 同温同压下,气体X和气体Y密度之比为b:a | |
| C. | 同物质的量的气体X和气体Y的质量之比为b:a | |
| D. | 25℃时,1 g气体X和1 g气体Y的分子数之比为b:a |
13.某酸碱指示剂(HIn)在水溶液中存在以下平衡,下列物质的溶液中,能使指示剂显蓝色的是( )
HIn(aq)?H++In-(aq)
(红色) (蓝色)
HIn(aq)?H++In-(aq)
(红色) (蓝色)
| A. | 稀硫酸 | B. | 醋酸 | C. | 稀氨水 | D. | 饱和食盐水 |
14.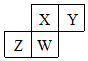 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
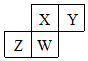 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Z的最高化合价分别与其主族序数相等 | |
| C. | 最高价氧化物对应水化物的酸性:Y>X>W | |
| D. | 最简单气态氢化物的热稳定性:Y>X>W>Z |