题目内容
下列化学用语的书写正确的是
A.NaH2PO4的水【解析】
H2PO4-+H2O H3O++HPO42-
H3O++HPO42-
B.H2S在水中的电离: H2S 2H++S2-
2H++S2-
C.Na2SO3的水【解析】
SO32-+H2O  HSO3-+OH-
HSO3-+OH-
D.CH3COONa在水中的电离:CH3COONa  CH3COO- + Na+
CH3COO- + Na+
C
【解析】
试题分析:A、NaH2PO4的水【解析】
H2PO4-+H2O OH-+H3PO4, A错误; B、H2S在水中的电离要分步电离: H2S
OH-+H3PO4, A错误; B、H2S在水中的电离要分步电离: H2S H++HS-,HS-
H++HS-,HS-  H++S2-,B错误;C、Na2SO3的水【解析】
H++S2-,B错误;C、Na2SO3的水【解析】
SO32-+H2O  HSO3-+OH-,C正确;D、CH3COONa在水中的电离:CH3COONa =CH3COO- + Na+,D错误;答案选C。
HSO3-+OH-,C正确;D、CH3COONa在水中的电离:CH3COONa =CH3COO- + Na+,D错误;答案选C。
考点:考查盐类水解与电离方程式。

(14分)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)  CH3OH(g) 下表为不同温度下的平衡常数(K)
CH3OH(g) 下表为不同温度下的平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
(1)该反应的平衡常数表达式K= ,ΔH 0(填“>”、“<”或“=”)。
(2)将1 mol的H2 和 1 mol 的 CO充入 1 L 恒容密闭反应器中,达到平衡后,容器内的压强为开始时的60%,求CO的平衡转化率(写出计算过程)。
(3)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是
(填字母)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡时c(H2)/ c(CH3OH)减小
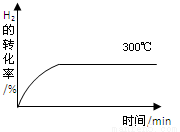
(4)其他条件相同时,在上述三个温度下分别发生该反应。300℃时,H2的转化率随时间的变化如图所示,请补充完成350℃时H2的转化率随时间的变化示意图。
 Cu+ H2O,该反应中( )
Cu+ H2O,该反应中( )