题目内容
9.含碳物质不完全燃烧会产生CO.利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.(1)已知COCl2分子中每个原子最外层都形成8电子的稳定结构,则一个COCl2分子内含有3个σ键1个π键.Fe(CO)5在一定条件下分解生成CO和铁.原子总数相同、价电子总数相同的分子,叫做等电子体,写出一个与CO是等电子体的分子N2,反应时中断裂的化学键是配位键.
(2)在合成氨的过程中,常因原料气中混有CO而使催化剂中毒.除去CO的化学方程式(HAc表示醋酸)为[Cu(NH3)2]Ac+CO+NH3═[Cu(NH3)3(CO)]Ac.在配合物[Cu(NH3)2]Ac中,中心离子是Cu+,配体是NH3,配位数是2.
分析 (1)COCl2分子中碳氧之间存在双键,结构式为: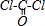 ,C=O键中含有1个δ键,1个π键,据此判断σ键数目,CO中有两个原子,价电子数为10,据此可判断出等电子体,Fe(CO)5在一定条件下分解生成CO和铁,断裂的是铁离子与CO之间的配位键;
,C=O键中含有1个δ键,1个π键,据此判断σ键数目,CO中有两个原子,价电子数为10,据此可判断出等电子体,Fe(CO)5在一定条件下分解生成CO和铁,断裂的是铁离子与CO之间的配位键;
(2)配合物中,配位体:提供孤电子对的分子或离子;中心离子:一般指接受电子对的原子;配位数:中心原子周围的配位原子个数.
配合物[Cu(NH3)2]Ac中,Ag+为中心离子,NH3为配体,配位数为2,外界是OH-,内界是[Ag(NH3)2]+,据此分析解答.
解答 解:(1)COCl2分子的结构式为: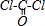 ,C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,根据原子总数相同、价电子总数相同的微粒互为等电子体,可知与CO分子等电子体的分子式为N2,Fe(CO)5在一定条件下分解生成CO和铁,断裂的是铁离子与CO之间的配位键,
,C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,根据原子总数相同、价电子总数相同的微粒互为等电子体,可知与CO分子等电子体的分子式为N2,Fe(CO)5在一定条件下分解生成CO和铁,断裂的是铁离子与CO之间的配位键,
故答案为:3;N2;配位键;
(2)配合物中,配位体:提供孤电子对的分子或离子;中心离子:一般指接受电子对的原子;配位数:中心原子周围的配位原子个数,所以在配合物[Cu(NH3)2]Ac中,Cu+为中心离子,NH3为配体,配位数为2,
故答案为:Cu+;NH3;2.
点评 本题考查了共价键的判断、等电子体、配合物的结构等知识点,难度不大,要学会运用等电子体原理书写等电子体,本题注重基础知识的考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列关于物质的性质或性质的比较的说法中,错误的是( )
| A. | 从晶体类型来看,晶体硅、水晶等物质都是原子晶体,所以具有较高的熔点 | |
| B. | 由于 HClO4(高氯酸)中的非羟基氧比HClO2(亚氯酸)中非羟基氧的多,所以高氯酸的酸性比亚氯酸的酸性强 | |
| C. | 成手性异构的化合物,在三维空间不能重叠,其物理化学性质却完全相同 | |
| D. | SO2分子中,S原子采用sp2杂化轨道成键,该分子的空间构型为平面三角形 |
1.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A. | 乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液,弃水层 | |
| B. | 苯(苯酚):加溴水,振荡,过滤除去沉淀 | |
| C. | 溴乙烷(乙醇):多次加水振荡,分液,弃水层 | |
| D. | 乙醇(水):加入新制生石灰,蒸馏,收集馏出物 |
18.向20mL2mol/LAlCl3溶液中加入30mLNaOH溶液,充分反应后得0.78g沉淀,则NaOH溶液的物质的量浓度为( )
| A. | 3mol/L | B. | 2mol/L | C. | 4mol/L | D. | 5mol/L |
 .
.