题目内容
化学与社会、生活密切相关.对下列现象或事实解释错误的是( )
| 选项 | 现象或事实 | 解释 |
| A | 明矾用于净水 | 铝离子水解产生的胶体具有很强吸附杂质的作用 |
| B | SO2能使品红溶液褪色 | SO2具有漂白性 |
| C | “地沟油”禁止食用,但可以用来制肥皂 | “地沟油”主要成分为油脂属于酯类可以发生皂化反应 |
| D | 用氯水和淀粉溶液鉴别食盐是否加碘 | 目前加碘食盐中含碘元素物质为KI |
| A、A | B、B | C、C | D、D |
考点:盐类水解的应用,二氧化硫的化学性质,油脂的性质、组成与结构,物质的检验和鉴别的基本方法选择及应用
专题:实验评价题
分析:A、明矾溶解后溶液中铝离子水解生成氢氧化铝胶体具有吸附性;
B、二氧化硫具有漂白性,选择性漂白;
C、地沟油”主要成分为油脂属于酯类可以发生皂化反应;
D、加碘实验时加入的KIO3;
B、二氧化硫具有漂白性,选择性漂白;
C、地沟油”主要成分为油脂属于酯类可以发生皂化反应;
D、加碘实验时加入的KIO3;
解答:
解:A、明矾溶解后溶液中铝离子水解生成氢氧化铝胶体具有吸附性,可以虚浮悬浮在水中的杂质起到净水作用,故A正确;
B、二氧化硫具有漂白性,选择性漂白可以使品红事业褪色,故B正确;
C、地沟油”主要成分为油脂属于酯类可以发生皂化反应,不能使用可以制备肥皂,故C正确;
D、加碘实验时加入的KIO3,不是KI,用氯水和淀粉不能借鉴是否加入碘元素,故D错误;
故选D.
B、二氧化硫具有漂白性,选择性漂白可以使品红事业褪色,故B正确;
C、地沟油”主要成分为油脂属于酯类可以发生皂化反应,不能使用可以制备肥皂,故C正确;
D、加碘实验时加入的KIO3,不是KI,用氯水和淀粉不能借鉴是否加入碘元素,故D错误;
故选D.
点评:本题考查了化学与生活中的化学知识分析判断,主要是物质性质的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
某原电池装置如图所示,下列有关叙述中,不正确的是( )
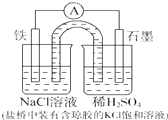

| A、Fe作负极,发生氧化反应 |
| B、盐桥的作用是平衡电荷,构成闭合回路 |
| C、工作一段时间后,NaCl溶液中c(Cl-)不变 |
| D、正极反应:2H++2e-=H2↑ |
下列推断合理的是( )
| A、Cu的活动性排在H之后,不能与浓H2SO4发生反应 |
| B、金刚石是自然界中硬度最大的物质,不能氧气发生反应 |
| C、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
某无色酸性溶液中能大量共存的离子组是( )
| A、K+、Mg2+、Cl-、NO3- |
| B、Ba2+、SO42-、Cl-、OH- |
| C、K+、OH-、CO32-、MnO4- |
| D、Ca2+、K+、Cl-、HCO3- |
NA表示阿伏加德罗常数.下列说法正确的是( )
| A、7.8 g Na2O2中含有的阴离子数目为0.2 NA |
| B、标准状况下,2.24 L CHCl3的分子数为0.1 NA |
| C、1 L 0.1 mol/L Al2(SO4)3溶液中,Al3+的数目为0.2 NA |
| D、0.1 mol Fe与足量稀HNO3反应,转移电子数为0.3NA |