题目内容
14.下列各组金属均有导线相连,并插入对应的液体中,其中不能组成原电池的是( )| A. | Zn|H2SO4(稀)|C | B. | Cu|AgNO3(aq)|Ag | C. | Zn|CCl4|Cu | D. | Fe|H2SO4(稀)|Cu |
分析 根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
解答 解:A、Zn|H2SO4(稀)|C,具备原电池的构成条件,所以能组成原电池,故A正确;
B、Cu|AgNO3(aq)|Ag,具备原电池的构成条件,所以能组成原电池,故B正确;
C、四氯化碳是非电解质,且不能自发的进行氧化还原反应,所以不能构成原电池,故C错误;
D、Fe|H2SO4(稀)|Cu,具备原电池的构成条件,所以能组成原电池,故D正确.
故选C.
点评 本题考查了原电池的构成条件,难度不大,根据原电池的构成条件即可解答本题.

练习册系列答案
相关题目
5.游泳池是公共场合,必须保持用水的清洁卫生,游泳池中的水常用漂白粉消毒,漂白粉的有效成分是( )
| A. | CaCl2 | B. | Ca(ClO)2 | C. | Ca(OH)2 | D. | HClO |
2.下列叙述正确的是( )
| A. | 若AgCl沉淀完全,就是指氯化银溶液中溶质离子的浓度为零 | |
| B. | 达到溶解平衡时,晶体就不再溶解 | |
| C. | 室温下,在100g水中能溶解1~10g的溶质,这种物质被称为可溶性物质 | |
| D. | 无机酸都是可溶的 |
9.下列变化过程中原物质分子内的共价键被破坏,同时有离子键形成的是( )
| A. | 碘升华 | B. | 盐酸和氢氧化钠溶液混合 | ||
| C. | 氯化氢溶于水 | D. | 氯化氢与氨气反应生成氯化铵固体 |
19.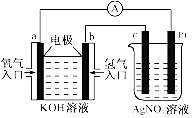 由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
 由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )
由化学能转变的热能或电能仍然是人类使用的主要能源.根据如图所示的装置,判断下列说法不正确的是( )| A. | 该装置中Pt极为阳极 | |
| B. | 当c极的质量变化了2.16g时,a极上消耗的O2在标准状况下的体积为1.12L | |
| C. | 该装置中b极的电极反应式是:H2+2OH--2e-=2H2O | |
| D. | 该装置中a极为正极,发生氧化反应 |
6.某温度下,水的电离平衡常数K电离=1.8×10-15,则该温度下,pH=12的强碱溶液与pH=2的强酸溶液混合(不考虑体积变化),所得混合溶液的pH=10,则强碱与强酸的体积比约为( )
| A. | 5.6﹕1 | B. | 9﹕1 | C. | 1﹕5.6 | D. | 1﹕9 |
3. 是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
 是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
| A. | B中含有的官能团有溴原子、碳碳双键 | |
| B. | A的结构简式是CH2=CHCH2CH3 | |
| C. | A能使酸性高锰酸钾溶液褪色 | |
| D. | ①②③的反应类型分别为加成反应、取代反应、消去反应 |
4.CPMA是蜂胶的活性成分,其结构简式如图所示,下列有关CPMA的叙述正确的是( )

| A. | CPMA的分子式为C17H18O4 | |
| B. | 1 mol CPMA中含有7 mol双键 | |
| C. | 1 mol CPMA最多可与2molNaOH反应 | |
| D. | CPMA能使酸性高锰酸钾溶液、溴水褪色 |