题目内容
汽车内燃机工作时产生的高温会引起N2和O2的反应:N2(g)+O2(g) ![]() 2NO(g),是导致汽车尾气中含有NO的原因之一。某同学对该反应进行研究。
2NO(g),是导致汽车尾气中含有NO的原因之一。某同学对该反应进行研究。
已知:反应a:N2(g)+O2(g) ![]() 2NO(g);△H1>0 K1=0.11
2NO(g);△H1>0 K1=0.11
反应b:NO(g)+CO(g) ![]() N2(g)+CO2(g);△H1<0 K2=1.64×105
N2(g)+CO2(g);△H1<0 K2=1.64×105
回答下列问题:
①要使上述两个反应中的K值相等,可采取的措施是 ;
A.降低反应a、b中NO的浓度
B.反应a、b采取不同的催化剂
C.反应a、b同时升高温度
D.反应a、b同时减小压强
②在一体积不变的密闭容器中,充入NO、CO提供条件使其按反应b进行反应。当NO、CO的起始浓度均为1.0mol?L―1,N2、CO2的超始浓度均为0时,NO的浓度、转化率随反应时间的变化如下列各图所示:
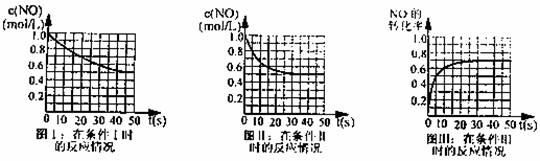
填写下列空白:反应条件I、II相比,可能的不同是 ;图III的平衡混合物中,CO2的浓度为 ;若上述反应只将NO、CO的起始浓度均改为2.0mol?L―1,仍然画出条件I~III下的NO的浓度、转化率随反应时间的变化图像,其中哪幅图像是不变的 。
①C;②催化剂;0.7mol?L―1;图III

练习册系列答案
相关题目

 汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.
汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一. 汽车内燃机工作时产生的高温会引起N2和O2的反应:N2(g)+O2(g)
汽车内燃机工作时产生的高温会引起N2和O2的反应:N2(g)+O2(g)
 2NO(g),这是汽车尾气中含有NO的原因之一。某同学为探究控制污染的方法,对该反应进行研究。
2NO(g),这是汽车尾气中含有NO的原因之一。某同学为探究控制污染的方法,对该反应进行研究。
 2NO(g)为________(填“吸热”或“放热”)反应。
2NO(g)为________(填“吸热”或“放热”)反应。