题目内容
使2.3g金属钠跟足量的水反应,反应后所得溶液的体积为500mL.试计算:
(1)反应后所得NaOH溶液的物质的量浓度是多少?
(2)反应生成的氢气在标准状况下的体积为多少毫升?
(1)反应后所得NaOH溶液的物质的量浓度是多少?
(2)反应生成的氢气在标准状况下的体积为多少毫升?
考点:化学方程式的有关计算
专题:计算题
分析:根据n=
计算Na的物质的量,根据方程式2Na+2H2O=2NaOH+H2↑,计算氢气、氢氧化钠物质的量,根据c=
计算氢氧化钠溶液物质的量的浓度,根据V=nVm计算氢气体积.
| m |
| M |
| n |
| V |
解答:
解:2.3gNa 的物质的量=
=0.1mol,
2 Na+2 H2O═2NaOH+H2↑
2 2 1
0.1mol n(NaOH) n(H2)
n(H2)=
n(Na)=0.05 mol
n(NaOH)=n(Na)=0.1 mol
(1)反应后所得NaOH溶液的物质的量浓度c=
=0.2mol/L,答:反应后所得NaOH溶液的物质的量浓度为0.2mol/L;
(2)反应生成的氢气在标准状况下的体积V=0.05mol×22400mL/mol=1120mL,答:反应生成的氢气在标准状况下的体积为1120mL.
| 2.3g |
| 23g/mol |
2 Na+2 H2O═2NaOH+H2↑
2 2 1
0.1mol n(NaOH) n(H2)
n(H2)=
| 1 |
| 2 |
n(NaOH)=n(Na)=0.1 mol
(1)反应后所得NaOH溶液的物质的量浓度c=
| 0.1mol |
| 0.5L |
(2)反应生成的氢气在标准状况下的体积V=0.05mol×22400mL/mol=1120mL,答:反应生成的氢气在标准状况下的体积为1120mL.
点评:本题考查化学方程式有关计算,比较基础,注意理解化学方程式表示的意义,有利于基础知识的巩固.

练习册系列答案
相关题目
下列各组实验中溶液最先变浑浊的是( )
| A、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度10℃ |
| B、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度10℃ |
| C、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度30℃ |
| D、0.2 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度30℃ |
下列说法正确的是( )
| A、已知a g乙烯气体充分燃烧时生成1 mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)═4CO2(g)+4H2O(l)△H=-4b kJ?mol-1 | ||||
| B、已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | ||||
C、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)
| ||||
| D、已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ?mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ?mol-1,则C(s,金刚石)═C(s,石墨)△H=-1.5 kJ?mol-1 |
国际无机化学命名委员会在1989年作出决定,把长式元素周期表原先的主副族及族号取消,由左至右改为18列.如IA为第1列,稀有气体元素为第18列.按此规定,下列说法中错误的是( )
| A、第9列元素中没有非金属元素 |
| B、第1列和第17列元素的单质熔、沸点变化趋势相反 |
| C、只有第2列元素原子的最外层有2个电子 |
| D、在整个18列元素中,第3列元素种类最多 |
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是( )
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| C、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| D、在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:Fe3+、NH4+、H+ |
已知酸性: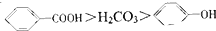 综合考虑反应物的转化率和原料成本等因素,将
综合考虑反应物的转化率和原料成本等因素,将 的最佳方法是( )
的最佳方法是( )
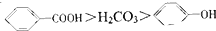 综合考虑反应物的转化率和原料成本等因素,将
综合考虑反应物的转化率和原料成本等因素,将 的最佳方法是( )
的最佳方法是( )| A、与稀H2SO4共热后,加入足量NaOH溶液 |
| B、与稀H2SO4共热后,加入足量NaHCO3溶液 |
| C、与足量的NaOH溶液共热后,再加入适量H2SO4 |
| D、与足量的NaOH溶液共热后,再通入足量CO2 |
某烃的结构简式为 分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )
分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )
 分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )
分子中处于四面体结构中心的碳原子数为a,一定在同一平面内的碳原子数为b,一定在同一直线上的碳原子数为c,则a,b,c依次为( )| A、4,5,3 |
| B、4,6,3 |
| C、2,4,5 |
| D、4,4,6 |
把aL含硫酸铵、硝酸铵的混合溶液分成两等份,一份用bmol烧碱刚好把NH3全部赶出,另一份与氯化钡溶液完全反应消耗cmolBaCl2,则原溶液中c(NO3-)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、用100ml 4mol/L盐酸与8.7gMnO2共热能制取氯气0.2NA |
| B、一定温度下0.1L 0.1mol/L的HA和1L0.01mol/L的HA所含A-微粒数均为0.01NA |
| C、4.5 gSiO2晶体中含有的硅氧键数目为0.3 NA |
| D、用Pt做电极电解硝酸铜溶液,当阳极产生的气体在标况下为22.4L,转移电子数目为NA |