题目内容
两种金属的混合物共15g,跟足量的盐酸反应时,恰好得到11.2L氢气(标况).下列各组金属不可能构成上述条件的混合物的是( )
| A、镁和银 | B、铜和锌 |
| C、锌和铁 | D、镁和铁 |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:假设金属都为+2价,根据M=
计算金属混合物的平衡相对原子质量,利用平均值法判断,若某一组分不反应,根据氢气计算反应金属的质量,反应金属的质量应小于15g.
| m |
| n |
解答:
解:11.2L氢气的物质的量为:
=0.5mol,
假设金属都为+2价,则金属混合物的平均相对原子质量为
=30,
A.Mg的相对原子质量为24,Ag与盐酸不反应,生成0.5mol氢气需要镁的质量为0.5mol×24g/mol=12g,符合题意,故A正确;
B.Zn的相对分子质量为65,Cu与稀硫酸不反应,生成0.5mol氢气所以Zn的质量为0.5mol×65g/mol=32.5g,大于15g,不符合题意,故B错误
C.Zn的相对分子质量为65,Fe的相对原子质量为56,平均值大于30,故C错误;
D.Mg的相对原子质量为24,Fe的相对原子质量为56,平均值可能为30,故D正确;
故选BC.
| 11.2L |
| 22.4L/mol |
假设金属都为+2价,则金属混合物的平均相对原子质量为
| 15 |
| 0.5 |
A.Mg的相对原子质量为24,Ag与盐酸不反应,生成0.5mol氢气需要镁的质量为0.5mol×24g/mol=12g,符合题意,故A正确;
B.Zn的相对分子质量为65,Cu与稀硫酸不反应,生成0.5mol氢气所以Zn的质量为0.5mol×65g/mol=32.5g,大于15g,不符合题意,故B错误
C.Zn的相对分子质量为65,Fe的相对原子质量为56,平均值大于30,故C错误;
D.Mg的相对原子质量为24,Fe的相对原子质量为56,平均值可能为30,故D正确;
故选BC.
点评:本题考查混合物的计算,难度中等,本题利用平均值法计算,注意化合价与相对原子质量的关系.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
相同温度下,体积均为1.5L的两个恒容容器中发生可逆反应:
X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ?mol-1,实验测得有关数据如表:
下列叙述不正确的是( )
X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ?mol-1,实验测得有关数据如表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
| A、容器①中达到平衡时,Y2的转化率为50% |
| B、Q=27.78kJ |
| C、若X2、Y2、XY3改按0、0、2投料,则达到平衡时吸热46.3KJ |
| D、若容器①体积改为1.0L.则达平衡时放出的热量小于46.3kJ |
人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实分析不正确的是( )
| A、亚硝酸盐是氧化剂 |
| B、维生素C是氧化剂 |
| C、亚硝酸盐将Fe3+还原成Fe2+ |
| D、维生素C被Fe3+氧化 |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温下,23g NO2 含有nA个氧原子 |
| B、0.1mol/L NaCl溶液含有0.1nA个Cl- |
| C、常温常压下,22.4L CCl4含有nA个CCl4分子 |
| D、含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1mol/L |
下列说法正确的是( )
A、按系统命名法,有机物 的命名为2,3,3,5,5.五甲基4,4二乙基己烷 的命名为2,3,3,5,5.五甲基4,4二乙基己烷 |
B、已知C-C键可以绕键轴自由旋转,结构简式为 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 |
| C、用溴水可以除去苯中混有的苯酚 |
| D、菜籽油、牛油、甘油等都属于酯,均能与氢氧化钠溶液发生皂化反应 |
在一定温度下,反应:2A(s)+2B(g)?C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )
| A、混合气的密度不再随时间而变化 |
| B、C的质量不再改变 |
| C、容器内的压强不随时间而变化 |
| D、单位时间内生成2a mol B,同时生成a molD |
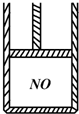 如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )
如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )| A、等于1.369g?L-1 |
| B、等于2.054g?L-1 |
| C、在1.369g?L-1和2.054g?L-1之间 |
| D、在2.054g?L-1和4.108g?L-1之间 |
下列能达到实验目的是( )
A、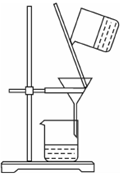 除去Fe(OH)3胶体中的FeCl3 |
B、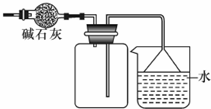 干燥、收集氨气,并吸收多余的氨气 |
C、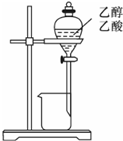 分离乙醇、乙酸 |
D、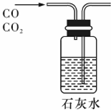 除去杂质气体二氧化碳 |
下列叙述正确的是( )
| A、1H和3H的质子数相同,它们是同种核素 |
| B、6Li和7Li的质子数相等,电子数也相等 |
| C、14C和14N的质量数相等,它们的中子数相等 |
| D、13C和14C属于同一种元素,它们的质量数相等 |