题目内容
2. 在容积一定温度一定的密闭容器中发生反应M2(?)+2R2(g)?M2R4(g),加入1mol M2和2molR2,反应过程中测得气体的平均相对分子质量随时间的变化如图所示.则下列说法错误的是( )
在容积一定温度一定的密闭容器中发生反应M2(?)+2R2(g)?M2R4(g),加入1mol M2和2molR2,反应过程中测得气体的平均相对分子质量随时间的变化如图所示.则下列说法错误的是( )| A. | M2既可能为固体,也可能为气体 | |
| B. | 达到平衡后,保持容器容枳和温度不变,再加入1molM2和2molR2,则R2转化率不变 | |
| C. | 达到平衡后,保持温度不变,将容器容积压缩到原来的一半,当达到新的平衡时,R2的浓度可能是原平衡时的1.8倍 | |
| D. | 若M2为气体,达到平衡后,保持容器容积和温度不变,再加入1molM2R4,则新的平衡时气体的平均相对分子质量增大 |
分析 A、如果M2为固体,随反应的进行,气体的质量增加,物质的量减小,所以混合气体的相对分子质量增大;如果M2为气体,气体的质量不变,物质的量减小,所以混合气体的相对分子质量增大;
B、再加入1molM2和2molR2,相当于增大压强;
C、达到平衡后,保持温度不变,将容器容积压缩到原来的一半,增大压强,平衡正向移动,如果不移动,R2的浓度可能是原平衡时的2倍,平衡正向移动,所以R2的浓度小于2倍;
D、若M2为气体,达到平衡后,保持容器容积和温度不变,再加入1molM2R4,等效于增大压强,平衡正向移动;
解答 解:A、如果M2为固体,随反应的进行,气体的质量增加,物质的量减小,所以混合气体的相对分子质量增大;如果M2为气体,气体的质量不变,物质的量减小,所以混合气体的相对分子质量增大,达平衡后不变,故A正确;
B、再加入1molM2和2molR2,相当于增大压强,平衡正向移动,则R2转化率变大,故B错误;
C、达到平衡后,保持温度不变,将容器容积压缩到原来的一半,增大压强,平衡正向移动,如果不移动,R2的浓度可能是原平衡时的2倍,平衡正向移动,所以R2的浓度小于2倍,所以可能是1.8倍,故C正确;
D、若M2为气体,达到平衡后,保持容器容积和温度不变,再加入1molM2R4,等效于增大压强,平衡正向移动,气体的质量不变,物质的量减小,所以混合气体的相对分子质量增大,故D正确;
故选B.
点评 本题考查化学平衡影响因素,为高频考点,明确改变容器体积时平衡如何移动是解本题关键,易错选项是C,注意将容器容积压缩到原来的一半,平衡不移动R2的物质的量是原来2倍,而压强改变,平衡移动,题目难度中等.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
12.下列有关表述正确的是( )
(1)-OH与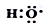 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
(2)次氛酸的电子式为:
(3)Mg2+的离子结构示意图:
(4)CO2的球棍模型示意图:
(5)熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4.
(1)-OH与
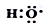 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同(2)次氛酸的电子式为:

(3)Mg2+的离子结构示意图:

(4)CO2的球棍模型示意图:

(5)熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4.
| A. | (1)(2) | B. | (3)(5) | C. | (4)(5) | D. | (1)(5) |
17.下列说法正确的是( )
| A. | 升高体系的温度或增加某一组分的浓度均能增加反应体系中活化分子所占百分数 | |
| B. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl反应中化学能只转变为热能 | |
| C. | 面粉生产工厂要求严禁烟火是因为面粉有机物颗粒极小,总表面积巨大容易被引燃爆炸 | |
| D. | 高锰酸钾受热分解是一个熵减小的过程 |
7.下列数据不一定随着温度升高而增大的是( )
| A. | 化学反应速率v | B. | 化学平衡常数K | ||
| C. | 弱电解质的电离平衡常数K | D. | 水的离子积常数Kw |
14.一定条件下,某容积不变的密闭容器内存在下列平衡:2HI(g)?H2(g)+I2(g);则下列有关说法正确的是( )
| A. | 如改变体系温度,体系颜色一定发生变化 | |
| B. | 如仅仅改变浓度这一条件,使得体系颜色加深,则上述平衡一定正移 | |
| C. | 继续充入HI气体,则HI的转化率将减小 | |
| D. | 温度不变时,当体系颜色变浅,则正反应速率和逆反应速率都将减小 |
7.下列说法不正确的是( )
| A. | 合金的硬度一般比各组分金属的低 | B. | 合金中可能含有非金属元素 | ||
| C. | 合金中肯定含有金属元素 | D. | 合金的熔点一般比各组分金属的低 |
