题目内容
3.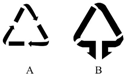 呵护生存环境,共建和谐社会是当今社会的主题.
呵护生存环境,共建和谐社会是当今社会的主题.①扬州市六圩污水处理厂三期工程不仅是“十二五”期间淮河流域水污染防治规划工程,也是我市今年重点减排项目.处理废水时加入明矾可作为混凝剂以吸附水中的杂质,明矾的化学式为KAl(SO4)2•12H2O;漂白粉能杀菌消毒,其作用原理可用化学方程式表示为2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O.
②现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为1:4.
③废旧的钢圈、轮胎应投入如图所示A(填“A”或“B”)标志的垃圾桶中.
④下列污水处理方法只涉及物理变化的是A.
A.过滤法 B.氧化还原法 C.中和法 D.化学沉淀法.
分析 ①明矾为KAl(SO4)2•12H2O,根据氯气与氢氧化钙反应的性质书写方程式;
②根据碳元素守恒计算物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比
③废旧的钢圈、轮胎都是可以再回收利用的物质;
④有新物质生成的变化属于化学变化,没有新物质生成的变化属于物理变化.
解答 解:①氯气和石灰水反应生成Ca(ClO)2、CaCl2和水,反应的方程式为2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,
故答案为:KAl(SO4)2•12H2O;2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O;
②根据碳元素守恒,可知乙醇完全燃烧产生二氧化碳n(CO2)=2n(C2H5OH),汽油(设为C8H18)完全燃烧产生的二氧化碳n′(CO2)=8n(C8H18),物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为n(CO2):n′(CO2)=2n(C2H5OH):8n(C8H18)=2:8=1:4;
故答案为:1:4;
③废旧的钢圈、轮胎都是可以再回收利用的物质,
故答案为:A;
④污水处理法中过滤是对不溶性固体和液体的分离,没有新物质生成,属于物理性质,而题中氧化还原反应、中和反应以及其它化学沉淀等方法,都有新物质生成,都属于化学变化;
故答案为:A.
点评 本题为综合题,涉及污水的处理方法、资源的回收利用、方程式的书写,明确物理变化与化学变化区别、明矾净水的原理、漂白粉的性质是解题关键,题难度不大.

练习册系列答案
相关题目
14.在含有大量的Ba2+、OH-、NO3- 的溶液中还可能大量存在的离子是( )
| A. | Na+ | B. | H+ | C. | SO42- | D. | NH4+ |
11.氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应生成H2和NaOH.下列叙述中,不正确的是( )
| A. | NaH的电子式为Na+[:H]- | |
| B. | NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 | |
| C. | 微粒半径H-<Li+ | |
| D. | NaH与H2O反应时,水作氧化剂 |
18.室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在澄清透明的溶液中:H+、Na+、SO42-、Cu2+ | |
| B. | 在$\frac{{K}_{w}}{c(O{H}^{-})}$=1 mol•L-1的溶液中:Na+、NH4+、I-、CO32- | |
| C. | 在0.1mol•L-1NaHSO4溶液中:K+、Fe2+、C1-、NO3- | |
| D. | 在能使甲基橙显黄色的溶液中:Ca2+、Ba2+、Br-、C1- |
8.下列说法中正确的是( )
| A. | 含H+的溶液一定呈酸性 | |
| B. | pH=7的溶液一定呈中性 | |
| C. | c(OH-)═c(H+)的溶液一定呈中性 | |
| D. | 水中加入硫酸恢复至室温后,Kw=c(H+)•c(OH-)将变大 |
15.下列关于胶体和溶液的说法中,正确的是( )
| A. | 胶体和溶液具有相同的性质:均一、稳定,静置后不产生沉淀 | |
| B. | 布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分 | |
| C. | 可以利用丁达尔效应区分胶体和溶液 | |
| D. | 只有胶状的物质如胶水、果冻类的才能称为胶体 |
12. 电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)X的电极名称是阴极.
(2)若X、Y都是惰性电极,a是硝酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,Y极上的电极反应式为2H2O-4e-=4H++O2↑,一段时间后,在X极附近观察到的现象是有气泡,溶液变红.
(3)若X、Y都是惰性电极,a是足量的AgNO3溶液,写出电解过程的化学方程式4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3 ,电解一段时间,当电极上通过的电子为0.2mol时,阴极上生成物的质量为21.5g.
(4)若要用电镀方法在铁表面镀一层金属铜,应该选择的方案是D.
 电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)X的电极名称是阴极.
(2)若X、Y都是惰性电极,a是硝酸钠溶液,实验开始时,同时在两边各滴入几滴石蕊试剂,Y极上的电极反应式为2H2O-4e-=4H++O2↑,一段时间后,在X极附近观察到的现象是有气泡,溶液变红.
(3)若X、Y都是惰性电极,a是足量的AgNO3溶液,写出电解过程的化学方程式4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4HNO3 ,电解一段时间,当电极上通过的电子为0.2mol时,阴极上生成物的质量为21.5g.
(4)若要用电镀方法在铁表面镀一层金属铜,应该选择的方案是D.
| 方案 | X | Y | a溶液 |
| A | 铜 | 石墨 | CuSO4 |
| B | 铜 | 铁 | CuSO4 |
| C | 铁 | 铜 | Fe(NO3)3 |
| D | 铁 | 铜 | CuSO4 |
13.下列物质直接参与的过程与氧化还原反应有关的是( )
| A. | 用乙醚从黄花蒿中提取青蒿素 | |
| B. | 用浸有酸性高锰酸钾的硅藻土作水果保鲜剂 | |
| C. | 生石灰用作煤炭燃烧的固硫剂 | |
| D. | 服用阿司匹林出现水杨酸反应时用小苏打解毒 |