题目内容
8.某学生的实验报告所列出的下列数据中合理的是( )| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用pH计测得某稀盐酸的pH为1.54 | |
| C. | 用碱式滴定管量取20.3 mL烧碱溶液 | |
| D. | 用托盘天平称得某物质的质量为13.15g |
分析 A.量筒精确到0.1;
B.pH计精确到0.01;
C.滴定管精确到0.01;
D.托盘天平精确到0.1.
解答 解:A.量筒精确到0.1,无法量取7.13mL稀盐酸,故A错误;
B.pH计精确到0.01,可pH计测得某稀盐酸的pH为1.54,故B正确;
C.滴定管精确到0.01,可量取20.3mL烧碱溶液,故C正确;
D.托盘天平精确到0.1,无法称量13.15g,故D错误.
故选BC.
点评 本题考查化学实验的基本操作,题目难度不大,注意相关基本实验操作的实验注意事项.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
19.1-乙氧基萘常用作香料,也可合成其他香料.实验室制备1-乙氧基萘的过程如图1:
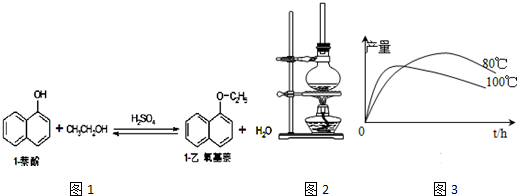
已知:1-萘酚的性质与苯酚相似,有难闻的苯酚气味.相关物质的物理常数:
(1)将72g 1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合.将混合液置于如图2所示的容器中加热充分反应.实验中使用过量乙醇的原因是提高1-萘酚的转化率.
(2)装置中长玻璃管的作用是:冷凝回流.
(3)该反应能否用实验室制备乙酸乙酯的装置不能(选填“能”或“不能”),简述理由产物沸点大大高于反应物乙醇,会降低产率.
(4)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层.为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤.正确的顺序是a(选填编号).
a.③②④①b.①②③④c.②①③④
(5)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图3所示,时间延长、温度升高,1-乙氧基萘的产量下降可能的两个原因是1-萘酚被氧化,温度高乙醇大量挥发或温度高发生副反应.
(6)提纯的产品经测定为43g,本实验中1-乙氧基萘的产率为50%.

已知:1-萘酚的性质与苯酚相似,有难闻的苯酚气味.相关物质的物理常数:
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
(2)装置中长玻璃管的作用是:冷凝回流.
(3)该反应能否用实验室制备乙酸乙酯的装置不能(选填“能”或“不能”),简述理由产物沸点大大高于反应物乙醇,会降低产率.
(4)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层.为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤.正确的顺序是a(选填编号).
a.③②④①b.①②③④c.②①③④
(5)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图3所示,时间延长、温度升高,1-乙氧基萘的产量下降可能的两个原因是1-萘酚被氧化,温度高乙醇大量挥发或温度高发生副反应.
(6)提纯的产品经测定为43g,本实验中1-乙氧基萘的产率为50%.
16.实验室用5%的NaOH溶液洗涤硝基苯以除去其中的酸性杂质,洗涤时不要用到( )
| A. | 漏斗 | B. | 分液漏斗 | C. | 烧杯 | D. | 滤纸 |
3.钛元素的外围电子排布为3d24s2. 实验室利用反应TiO2(s)+CCl4(g)$\stackrel{△}{→}$ TiCl4(g)+CO2(g)制取TiCl4,装置如下:
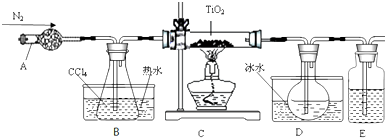
有关物质的性质如下表.
(1)装置E中的试剂是浓硫酸.反应结束前进行如下操作:
①停止通氮气 ②熄灭酒精灯 ③冷却至室温
正确的顺序为②③①(填序号).
(2)欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(3)TiCl4 遇到湿空气发生强烈水解,其中一种物质是TiO(OH)2,试写出该水解反应的化学方程式TiCl4+3H2O=TiO(OH)2+4HCl.
(4)有同学认为该反应还会生成CO,所以要增加尾气吸收装置,试分析该观点的合理性不合理;因为不会发生氧化还原反应
(5)也可以用反应TiO2(s)+2C(s)+2Cl2(g) $\stackrel{△}{→}$TiCl4(g)+2CO(g) 制取TiCl4,在上述实验装置中将通氮气改为通氯气,撤去装置B,请简述对该装置的其它改变处石英管内改为盛TiO2和C;将E改为盛碱石灰的干燥管;增加CO的吸收装置(答橡胶袋、盛醋酸亚铜氨的洗气瓶等均可).

有关物质的性质如下表.
| 物质 | 熔点/℃ | 沸点/℃ | 其它 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
①停止通氮气 ②熄灭酒精灯 ③冷却至室温
正确的顺序为②③①(填序号).
(2)欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(3)TiCl4 遇到湿空气发生强烈水解,其中一种物质是TiO(OH)2,试写出该水解反应的化学方程式TiCl4+3H2O=TiO(OH)2+4HCl.
(4)有同学认为该反应还会生成CO,所以要增加尾气吸收装置,试分析该观点的合理性不合理;因为不会发生氧化还原反应
(5)也可以用反应TiO2(s)+2C(s)+2Cl2(g) $\stackrel{△}{→}$TiCl4(g)+2CO(g) 制取TiCl4,在上述实验装置中将通氮气改为通氯气,撤去装置B,请简述对该装置的其它改变处石英管内改为盛TiO2和C;将E改为盛碱石灰的干燥管;增加CO的吸收装置(答橡胶袋、盛醋酸亚铜氨的洗气瓶等均可).
13.氮氧化铝(AlON)是一种空间网状结构,硬度大熔点高的透明材料,描述正确的是( )
| A. | 含有离子键 | B. | 属于原子晶体 | ||
| C. | 既有离子键又有共价键 | D. | 属于离子晶体 |
20.化学反应时,反应物的量不同,产物或现象可能会发生变化.下列正确的是( )
| A. | 硫在少量氧气中燃烧成SO2,过量能生成SO3 | |
| B. | 铁丝在少量氯气中燃烧生成FeCl2,过量则生成FeCl3 | |
| C. | 氯水滴入淀粉碘化钾稀溶液中,少量氯水有蓝色,过量蓝色消失 | |
| D. | NaClO溶液中通少量CO2生成Na2CO3和HClO,过量生成NaHCO3和HClO |
17.化学与生活密切相关,下列应用中利用了物质氧化性的是( )
| A. | 明矾净化水 | B. | 纯碱去油污 | C. | 食醋除水垢 | D. | 双氧水消毒 |
18.下列有机物中,所有的碳原子不可能都共面的是( )
| A. | 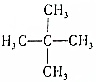 | B. | 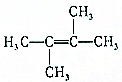 | C. | 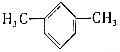 | D. | 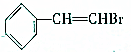 |