题目内容
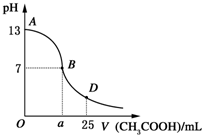 I.如图所示,向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.请回答:
I.如图所示,向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.请回答:(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?
(2)某温度下,若取上述二者恰好完全反应所得的溶液若干体积,向其中逐滴滴加等浓度的HCl溶液,则下列关系一定正确的是
A.c(H+)?c(OH-)=1×10-14
B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
C.c(Na+)=c(CH3COOH)+c(CH3COO-)
D.c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是
A.c(OH-)大于c(CH3COO-) B.c(OH-)小于c(CH3COO-)
C.c(OH-)等于c(CH3COO-) D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)
(5)如果使用NaOH溶液和CH3COOH溶液完成滴定实验,从下列选项中选出最恰当的一项
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 酚酞 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 石蕊 | (乙) |
滴定时一般左手
A.轻轻转动酸式滴定管的活塞
B.轻轻挤压碱式滴定管的玻璃球
C.摇动锥形瓶
D.滴定管内液面的变化
E.锥形瓶内溶液颜色的变化
读数时,目光应与凹液面的最
Ⅱ.t℃时,某稀硫酸溶液中c(H+)=10-amol?L-1,c(OH-)=10-bmol?L-1,已知a+b=13,则该温度下水的离子积常数Kw的数值为
考点:酸碱混合时的定性判断及有关ph的计算,pH的简单计算,中和滴定
专题:实验题,电离平衡与溶液的pH专题
分析:Ⅰ.(1)氢氧化钠和醋酸溶液按照物质的量之比1:1反应生成的醋酸钠为强碱弱酸盐,溶液显碱性,pH>7;
(2)温度不知,无法确定氢离子与氢氧根离子乘积;加入氯化氢后溶液中含有氯离子,电荷守恒漏掉了氯离子的浓度;加入的盐酸溶液体积不确定,则氯离子浓度大小不能确定;无论加入多少盐酸,一定满足物料守恒c(Na+)=c(CH3COOH)+c(CH3COO-);
(3)在AB区间内,包括CH3COOH和NaOH恰好完全反应以及CH3COOH不足,氢氧化钠溶液过量溶液显碱性两种可能性;
(4)在D点时,NaOH和CH3COOH反应后剩余CH3COOH,溶液的组成为等浓度的CH3COOH和CH3COONa的混合物;
(5)根据本实验是酸滴定碱,酸式滴定管用来盛放酸,碱式滴定管用来盛放碱,强酸滴定弱碱时应选用酚酞作指示剂来分析;
(6)根据中和滴定中左手、右手、眼睛、读数等正确的操作方法进行解答;
Ⅱ.根据水的离子积常数Kw=c(H+)?c(OH-)进行计算;根据计算得出酸碱反应后碱过量,根据反应后的剩余的碱的物质的量,求出c(OH-),然后根据水的离子积常数计算c(H+),最后求出pH.
(2)温度不知,无法确定氢离子与氢氧根离子乘积;加入氯化氢后溶液中含有氯离子,电荷守恒漏掉了氯离子的浓度;加入的盐酸溶液体积不确定,则氯离子浓度大小不能确定;无论加入多少盐酸,一定满足物料守恒c(Na+)=c(CH3COOH)+c(CH3COO-);
(3)在AB区间内,包括CH3COOH和NaOH恰好完全反应以及CH3COOH不足,氢氧化钠溶液过量溶液显碱性两种可能性;
(4)在D点时,NaOH和CH3COOH反应后剩余CH3COOH,溶液的组成为等浓度的CH3COOH和CH3COONa的混合物;
(5)根据本实验是酸滴定碱,酸式滴定管用来盛放酸,碱式滴定管用来盛放碱,强酸滴定弱碱时应选用酚酞作指示剂来分析;
(6)根据中和滴定中左手、右手、眼睛、读数等正确的操作方法进行解答;
Ⅱ.根据水的离子积常数Kw=c(H+)?c(OH-)进行计算;根据计算得出酸碱反应后碱过量,根据反应后的剩余的碱的物质的量,求出c(OH-),然后根据水的离子积常数计算c(H+),最后求出pH.
解答:
解:Ⅰ.(1)溶液混合后发生的反应为:NaOH+CH3COOH=CH3COONa+H20,当醋酸和氢氧化钠的物质的量之比为1:1时,反应生成的CH3COONa为强碱弱酸盐,溶液显碱性,pH>7,介于AB之间,
故答案为:否、AB;
(2)A.c(H+)?c(OH-)=1×10-14,温度没有确定,则水的离子积不一定为1×10-14,故A错误;
B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-),加入氯化氢后,溶液中多了氯离子,则电荷守恒不能漏掉氯离子的浓度,故B错误;
C.c(Na+)=c(CH3COOH)+c(CH3COO-),无论加入多少氯化氢溶液,一定存在:c(Na+)=c(CH3COOH)+c(CH3COO-),故C正确;
D.c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-),由于加入的氯化氢溶液体积没有确定,则氯离子的浓度大小无法确定,故D错误;
故答案为:C;
(3)在AB区间内,c(OH-)>c(H-),说明溶液显碱性,当NaOH和CH3COOH恰好反应时,显碱性,此时生成的溶液可能为醋酸钠,c(OH-)小于c(CH3COO-);当NaOH和CH3COOH反应后剩余NaOH,溶液仍然显碱性,此时若剩余的NaOH量很大,则c(OH-)大于c(CH3COO-),也有可能剩余的NaOH和CH3COONa中CH3COO-水解之后剩余的CH3COO-的浓度相等,所以D正确,
故答案为:D;
(4)在D点时,反应后CH3COOH剩余,溶液的组成为等浓度的CH3COOH和CH3COONa的混合物,根据物料守恒,此时:c(CH3COO-)+c(CH3COOH)=2c(Na+),
故答案为:=,
(5)甲为酸式滴定管,乙为碱式滴定管,酸滴定碱,酸盛放在酸式滴定管中,指示剂选用酚酞,故C正确,
故答案为:C;
(6)中和滴定时,左手应该轻轻转动酸式滴定管的活塞,右手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色的变化,以便及时判断滴定终点;读数时目光应与凹液面的最下端保持水平,
故答案为:A;C;E;下;
Ⅱ.水的离子积常数为:Kw=c(H+)?c(OH-)=10-a×10-b=10-(a+b)=10-13;
稀H2SO4溶液与NaOH反应的关系式:H2SO4~2NaOH
1 2
100mL×0.1mol?L-1=0.01mol 100mL×0.4mol?L-1=0.04
显然碱过量,过量的氢氧根离子的物质的量为:0.04mol-0.01mol×2=0.02mol,
则混合液中:c(OH-)=
=0.1mol/L,
所以c(H+)=
mol/L=10-12mol?L-1,
溶液的pH=12,
故答案为:10-13;12.
故答案为:否、AB;
(2)A.c(H+)?c(OH-)=1×10-14,温度没有确定,则水的离子积不一定为1×10-14,故A错误;
B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-),加入氯化氢后,溶液中多了氯离子,则电荷守恒不能漏掉氯离子的浓度,故B错误;
C.c(Na+)=c(CH3COOH)+c(CH3COO-),无论加入多少氯化氢溶液,一定存在:c(Na+)=c(CH3COOH)+c(CH3COO-),故C正确;
D.c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-),由于加入的氯化氢溶液体积没有确定,则氯离子的浓度大小无法确定,故D错误;
故答案为:C;
(3)在AB区间内,c(OH-)>c(H-),说明溶液显碱性,当NaOH和CH3COOH恰好反应时,显碱性,此时生成的溶液可能为醋酸钠,c(OH-)小于c(CH3COO-);当NaOH和CH3COOH反应后剩余NaOH,溶液仍然显碱性,此时若剩余的NaOH量很大,则c(OH-)大于c(CH3COO-),也有可能剩余的NaOH和CH3COONa中CH3COO-水解之后剩余的CH3COO-的浓度相等,所以D正确,
故答案为:D;
(4)在D点时,反应后CH3COOH剩余,溶液的组成为等浓度的CH3COOH和CH3COONa的混合物,根据物料守恒,此时:c(CH3COO-)+c(CH3COOH)=2c(Na+),
故答案为:=,
(5)甲为酸式滴定管,乙为碱式滴定管,酸滴定碱,酸盛放在酸式滴定管中,指示剂选用酚酞,故C正确,
故答案为:C;
(6)中和滴定时,左手应该轻轻转动酸式滴定管的活塞,右手摇动锥形瓶,眼睛观察锥形瓶内溶液颜色的变化,以便及时判断滴定终点;读数时目光应与凹液面的最下端保持水平,
故答案为:A;C;E;下;
Ⅱ.水的离子积常数为:Kw=c(H+)?c(OH-)=10-a×10-b=10-(a+b)=10-13;
稀H2SO4溶液与NaOH反应的关系式:H2SO4~2NaOH
1 2
100mL×0.1mol?L-1=0.01mol 100mL×0.4mol?L-1=0.04
显然碱过量,过量的氢氧根离子的物质的量为:0.04mol-0.01mol×2=0.02mol,
则混合液中:c(OH-)=
| 0.02mol |
| 0.2L |
所以c(H+)=
| 1×10-13 |
| 0.1 |
溶液的pH=12,
故答案为:10-13;12.
点评:本题考查了酸碱混合的定性判断、酸碱中和滴定、溶液pH的计算等知识,题目难度中等,试题题量较大,知识点较多,注意掌握中和滴定原理及正确的操作方法,明确溶液酸碱性与溶液pH的计算方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
随着卤素原子半径的增大,下列递变规律正确的是( )
| A、单质的熔、沸点逐渐降低 |
| B、卤素离子的还原性逐渐增强 |
| C、单质的氧化性逐渐增强 |
| D、气态氢化物的稳定性逐渐增强 |
下列叙述不正确的是( )
| A、乙醇、乙烯和植物油都能使酸性高锰酸钾褪色 |
| B、乙醇、乙烷、乙酸都可以与钠反应生成氢气 |
C、聚丙烯的结构简式为: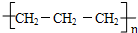 |
| D、用灼烧闻气味的方法可以区分纯棉织物和纯毛织物 |
已知碳酸、亚硫酸、次氯酸的平衡常数如表,下列说法正确的是( )
| H2CO3 | H2SO3 | HClO |
| K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A、相同条件下,同浓度的NaClO溶液和Na2CO3溶液的碱性,前者更强 |
| B、Na2CO3溶液中通少量SO2:2CO32-+SO2+H2O═2HCO3-+SO32- |
| C、NaHCO3溶液中通少量SO2:2HCO3-+SO2═CO2+SO32-+H2O |
| D、向氯水中分别加入等浓度的NaHCO3和NaHSO3溶液,均可提高氯水中HClO的浓度 |
25℃时,将a mol/L的氨水与b mol/L盐酸等体积混合,下列有关推论不正确的是( )
| A、若混合后溶液pH=7,则c(NH4+)═c(Cl-) |
| B、若b=2a,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、若a=2b,则(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、若混合后溶液满足c(H+)═c(OH-)+c(NH3?H2O),则可推出a=b |
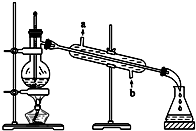 甘油的分离
甘油的分离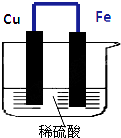 如图所示,将铁、铜通过导线相连,置于稀硫酸中.
如图所示,将铁、铜通过导线相连,置于稀硫酸中.