题目内容
18.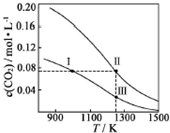 在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1mol CO2和0.2mol CO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1mol CO2和0.2mol CO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )| A. | 化学平衡常数K:K(状态Ⅰ)<K(状态Ⅱ)<K(状态Ⅲ) | |
| B. | CO2的平衡转化率α:α(状态Ⅰ)<α(状态Ⅱ)=α(状态Ⅲ) | |
| C. | 体系中c(CO):c (CO,状态Ⅱ)<2c (CO,状态Ⅲ) | |
| D. | 逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ) |
分析 A.状态II、状态Ⅲ的温度相同,状态II看作先加入0.1molCO2,与状态Ⅲ平衡时CO的浓度相同,再加入0.1molCO2,若平衡不移动,Ⅱ状态CO的浓度等于2倍Ⅲ,但再充入CO2,相当增大压强,平衡左移动,消耗CO;
B.由图象可知,状态Ⅱ和状态Ⅲ平衡时CO2的浓度不同;
C.状态II、状态Ⅲ的温度相同,状态II看作先加入0.1molCO2,与状态Ⅲ平衡时CO的浓度相同,再加入0.1molCO2,若平衡不移动,Ⅱ状态CO的浓度等于2倍Ⅲ,但再充入CO2,相当增大压强,平衡左移动,消耗CO;
D.状态I、状态Ⅲ的温度不同,温度高反应速率快.
解答 解:A.状态II、状态Ⅲ的温度相同,所以KⅡ=KⅢ,又由图中温度高平衡时c(CO2)小,则升高温度平衡正向移动,则温度高K大,所以KⅠ<KⅡ=KⅢ,故A错误;
B.由图象可知,状态Ⅱ和状态Ⅲ平衡时CO2的浓度不同,所以转化率不同,故B错误;
C.状态II、状态Ⅲ的温度相同,状态II看作先加入0.1molCO2,与状态Ⅲ平衡时CO的浓度相同,再加入0.1molCO2,若平衡不移动,Ⅱ状态CO的浓度等于2倍Ⅲ,但再充入CO2,相当增大压强,平衡左移,消耗CO,则c(CO,状态Ⅱ)<2c(CO,状态Ⅲ),故C正确;
D.状态I、状态Ⅲ的温度不同,温度高反应速率快,则逆反应速率为V逆(状态Ⅰ)<V逆(状态Ⅲ),故D错误;
故选C.
点评 本题考查化学平衡及平衡的建立,为高频考点,把握平衡移动的影响因素、图象分析为解答的关键,选项B为解答的难点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列有关叙述正确的是( )
| A. | “煤改气”、“煤改电”等改造工程有利于减少雾霾天气 | |
| B. | PM2.5含有的铅、镉、铬、钒、砷等元素均为对人体有害的金属元素 | |
| C. | 田间焚烧秸秆易造成灰霾,灰霾粒子平均直径在1000~2000nm之间,能发生丁达尔效应 | |
| D. | 汽车尾气净化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
9.下列物质中属于碱性氧化物的是( )
| A. | CO2 | B. | CuO | C. | H2O | D. | Ca(OH)2 |
6.有机物甲能发生银镜反应,甲经催化加氢还原为乙,1mol乙与足量钠反应产生氢气22.4L(标准状况下),据此推断乙可能是( )
| A. | CH3-CH2-OH | B. | CH3-CH2-CH2-OH | ||
| C. | HO-CH2-CH2-CH2-OH | D. |  |
13.现有Na2CO3、H2SO4、Ba(OH)2三种物质的量浓度与体积都相等的溶液,若以不同顺序将它们中的两种混合起来,出现沉淀后过滤,再将滤液与第三种溶液混合起来,最终所得的溶液( )
| A. | 可能呈酸性 | B. | 可能呈中性 | C. | 一定呈碱性 | D. | 一定呈中性 |
4.目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究.已知在不同温度下的化学反应.平衡常数(K1、K2、K3)如表所示:
请回答下列问题:
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1×K2(用K1、K2表示).
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有BC(填字母序号).
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
(5)甲醇是重要的基础化工原料,又是一种新型的燃料,最近有人制造了一种燃料电池,一个电极通入空气,另一个电极加入甲醇,电池的电解质是掺杂了Y2O3的ZrO2晶体,它们在高温下能传导O2-离子,该电池的正极反应式为O2+4e-=2O2-.电池工作时,固体电解质里的O2-向负极移动.
(6)300℃时,在一定的压强下,5molCO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
下列说法正确的是D.
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
| ①2H2(g)+CO(g)?CH3OH(g) | △H1 | K1 | 2.5 | 0.34 | 0.15 |
| ②CO2(g)+H2(g)?CO(g)+H2(g) | △H2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g)?CH3OH(g)+H2(g) | △H3 | K3 | |||
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1×K2(用K1、K2表示).
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有BC(填字母序号).
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
(5)甲醇是重要的基础化工原料,又是一种新型的燃料,最近有人制造了一种燃料电池,一个电极通入空气,另一个电极加入甲醇,电池的电解质是掺杂了Y2O3的ZrO2晶体,它们在高温下能传导O2-离子,该电池的正极反应式为O2+4e-=2O2-.电池工作时,固体电解质里的O2-向负极移动.
(6)300℃时,在一定的压强下,5molCO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 平衡时数据 | CH3OH的浓度(mol/L) | C1 | C2 | C3 |
| 反应体系的能量变化 | aKJ | bKJ | cKJ | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | a1 | a2 | a3 | |
A.2c1>c3 B.a+b<90.8 C.2p2<p3 D.α1+α3<1.
 .
. .
.