题目内容
2.铁钉在下列情况下腐蚀最快的是( )| A. | 铁钉放在干燥的空气中 | B. | 铁钉完全浸没在植物油中 | ||
| C. | 铁钉一半浸没在食盐水中 | D. | 铁钉一半浸没在水中 |
分析 铁与氧气和水充分接触时容易生锈,水和氧气同时存在是铁生锈的必要条件,但是酸、盐溶液更能加速铁的锈蚀,据此解答.
解答 解:A、在干燥的空气中,铁与水不接触,不易生锈;
B、浸没在植物油中,铁与水和氧气都不接触,不易生锈;
C、铁钉一半浸没在食盐水中,形成原电池,易生锈,盐溶液更能加速铁的腐蚀;
D、铁钉一半浸没在水中,铁与水和氧气同时接触,易生锈,但没有食盐水中腐蚀快;
故选C.
点评 本题考查的是铁的生锈的条件,铁与氧气和水充分接触时容易生锈,酸、盐溶液更能加速铁的锈蚀.

练习册系列答案
相关题目
12.下列离子反应方程式中,错误的是( )
| A. | 将氨通入盐酸中:NH3+H+═NH4+ | |
| B. | 在NaOH溶液中滴入几滴NH4CI溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将少量铜粉放入浓硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 将稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
13.化学与生活、生产密切相关,下列有关说法正确的是( )
| A. | 硅晶体具有半导体性能,可用于制取光导纤维 | |
| B. | 二氧化硫可以漂白纸浆 | |
| C. | 硅酸可以用于刻蚀玻璃 | |
| D. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
10.下列化学方程式中,属于水解反应的是( )
| A. | CH3COOH+H2O?CH3COO-+H3O+ | B. | HS-+H2O?S2-+H3O+ | ||
| C. | CO2+H2O?HCO3-+H+ | D. | CO32-+H2O?HCO3-+OH- |
17.下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入CO2至过量
②向Fe(OH)3胶体中逐滴加入稀盐酸至过量
③向NaAlO2 溶液中通入CO2至过量
④向 AlCl3溶液中加入 Ba(OH)2溶液至过量
⑤向CaCl2溶液中通入 CO2 至过量.
①向饱和碳酸钠溶液中通入CO2至过量
②向Fe(OH)3胶体中逐滴加入稀盐酸至过量
③向NaAlO2 溶液中通入CO2至过量
④向 AlCl3溶液中加入 Ba(OH)2溶液至过量
⑤向CaCl2溶液中通入 CO2 至过量.
| A. | ①③⑤ | B. | ①② | C. | ①③ | D. | ②③⑤ |
7.氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是( )
| A. | 35Cl原子所含质子数为18 | |
| B. | $\frac{1}{18}$mol的1H35Cl的分子所含中子数约为6.02×1023 | |
| C. | 3.5Cl2气体的体积约为22.4L | |
| D. | 35Cl2气体的摩尔质量为70 |
14.为了检验SO2的性质,下列实验现象、解释与结论均正确的是( )
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 将SO2气体通入KMnO4(H+)溶液中 | 溶液褪色 | SO2有漂白性 |
| B | 将SO2气体通入H2S溶液中 | 溶液变浑浊 | SO2有氧化性 |
| C | 将SO2气体通入紫色石蕊溶液中 | 溶液先变红色后褪色 | SO2是酸性氧化物 |
| D | 将SO2气体通入Ca(ClO)2溶液中 | 溶液变浑浊 | 亚硫酸的酸性比次氯酸的酸性强 |
| A. | A | B. | B | C. | C | D. | D |
11.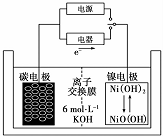 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
 一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )
一种二次电池如图所示,该电池的电解质为强碱溶液,下列说法中正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为原电池的负极 | |
| D. | 放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O |
19.已知(1)H2O(g)=H2O(l)△H1=-Q1 kJ•mol-1
(2)CH3OH(g)=CH3OH(l)△H2=-Q2 kJ•mol-1
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H3=-Q3 kJ•mol-1
(Q1、Q2、Q3均大于0)若使1mol液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)( )
(2)CH3OH(g)=CH3OH(l)△H2=-Q2 kJ•mol-1
(3)2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H3=-Q3 kJ•mol-1
(Q1、Q2、Q3均大于0)若使1mol液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)( )
| A. | Q1+Q2+Q3 | B. | 0.5Q3-Q2+2Q1 | C. | Q3-2Q2+4Q1 | D. | 0.5(Q1+Q2+Q3) |