题目内容
硫代硫酸钠(Na2S2O3)俗称大苏打或海波,是无色或淡黄色结晶,能风化和潮解,纯品可作照相定影剂、去氯剂和分析试剂,还用于皮革、纺织等工业.
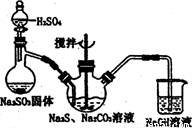
(1)工业上制取硫代硫酸钠(Na2S2O3),用Na2SO3和硫粉在水溶液中加热反应而得到.但在混合前,一般先用少许乙醇浸润,其原因是什么?
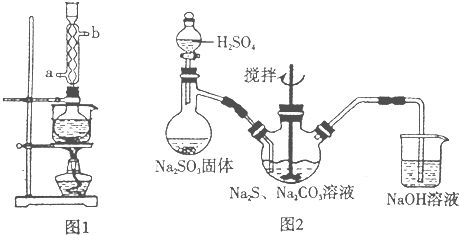
(2)又知:Na2S2O3+H2SO4![]() S↓+SO2↑+H2O+Na2SO4通过析出硫的速率可以说明反应速率的快慢,请判断下列几种情况下,最先看到硫析出的是( )
S↓+SO2↑+H2O+Na2SO4通过析出硫的速率可以说明反应速率的快慢,请判断下列几种情况下,最先看到硫析出的是( )

(3)对于上述反应,如果温度每升高10℃,反应速率增加为原来的3倍.那么20℃时看到沉淀开始析出的时间需54 s,若将温度提高到50℃,看到沉淀开始析出的时间需________s.
答案:
解析:
解析:
(1)硫不溶于水,很难与Na2SO3溶液接触而反应,当用乙醇湿润后,因乙醇易溶于水,增加了硫粉与水的接触面积,从而提高了反应速率,增加了Na2S2O3的日产量. (2)C (3)2
[提示:(1)硫用乙醇湿润后,因乙醇易溶于水,增加了硫粉与水的接触面积,从而提高了反应速度.(2)反应速率最快的肯定是温度最高、反应物浓度最大的一组.即上述的C组.(3)解此问要弄清两个关系:即时间与速率的关系、速度与温度的关系.由20℃升至50℃,共升高30℃,速率增加到原来的33倍,故耗时为2s.]

练习册系列答案
相关题目