题目内容
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中
A.至少存在5种离子
B.Cl-一定存在,且c(Cl‑)≥0.4mol/L
C.SO42-、NH4+一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在, K+可能存在
【答案】
B
【解析】
试题分析:原溶液中加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀,说明原溶液中一定存在NH4+、Fe3+,且它们的物质的量都为0.02mol,则CO32-一定不存在,Al3+不能确定;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀,说明原溶液中一定存在SO42-,且SO42-离子的物质的量为0.02mol,则一定存在的离子是NH4+、Fe3+、SO42-;根据溶液中符合电荷守恒规律,所以原溶液中一定存在Cl-,且c(Cl‑)≥0.4mol/L。A、至少存在4种离子,错误;B、正确;C、Cl-一定存在,错误;D、Al3+可能存在,错误,答案选B。
考点:考查溶液中的离子的鉴定

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A、至少存在5种离子 | B、Cl-一定存在,且c(Cl?)≥0.4mol/L | C、SO42-、NH4+、一定存在,Cl-可能不存在 | D、CO32-、Al3+一定不存在,K+可能存在 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+.某同学为了确认其成分,取部分试液,设计并完成了如下实验:由此可知原溶液中( )
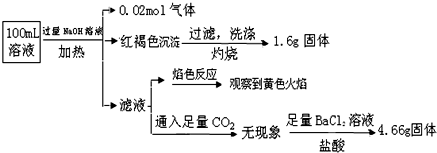

| A、原溶液中c(Fe3+)=0.2mol?L-1 | B、要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+ | C、SO42-、NH4+、Na+一定存在,CO32-、Al3+一定不存在 | D、溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol?L-1 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+ 和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A、NH4+、Fe3+一定存在,K+可能存在 | B、Cl-=一定存在,且c(Cl-)≤0.4 mol/L | C、SO42-、NH4+、Fe3+一定存在,且物质的量浓度均为0.02 mol/L | D、CO32-、Al3+一定不存在,K+ 一定存在 |