题目内容
14.下表是几种弱酸常温下的电离平衡常数:| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
| A. | 碳酸的酸性强于氢硫酸 | |
| B. | 多元弱酸的酸性主要由第一步电离决定 | |
| C. | 常温下,加水稀释醋酸,$\frac{c(C{H}_{3}CO{O}^{-})}{c(CHCOOH)•c(O{H}^{-})}$增大 | |
| D. | 向弱酸溶液中加少量NaOH溶液,电离常数不变 |
分析 A.由表格数据可知,碳酸的K1>氢硫酸的K1;
B.多元弱酸分步电离,以第一步为主;
C.$\frac{c(C{H}_{3}CO{O}^{-})}{c(CHCOOH)•c(O{H}^{-})}$=$\frac{Ka}{Kw}$,Ka、Kw均只与温度有关;
D.弱酸的电离平衡常数与温度有关,与浓度无关.
解答 解:A.由表格数据可知,碳酸的K1>氢硫酸的K1,则碳酸的酸性强于氢硫酸,故A正确
B.多元弱酸分步电离,以第一步为主,则多元弱酸的酸性主要由第一步电离决定,故B正确;
C.常温下,加水稀释醋酸,$\frac{c(C{H}_{3}CO{O}^{-})}{c(CHCOOH)•c(O{H}^{-})}$=$\frac{Ka}{Kw}$,则$\frac{c(C{H}_{3}CO{O}^{-})}{c(CHCOOH)•c(O{H}^{-})}$不变,故C错误;
D.弱酸的电离平衡常数与温度有关,与浓度无关,则向弱酸溶液中加少量NaOH溶液,电离常数不变,故D正确;
故选C.
点评 本题考查弱电解质的电离平衡,为高频考点,把握电离平衡常数的影响因素、酸性比较为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的难点,题目难度不大.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
5. 某研究性学习小组对同学们常用的三种品牌牙膏中摩擦剂成分进行调查,结果如表:
某研究性学习小组对同学们常用的三种品牌牙膏中摩擦剂成分进行调查,结果如表:
(1)某品牌透明牙膏的摩擦剂二氧化硅属于酸性(填酸性、碱性或两性)氧化物,其常作为工业制备晶体硅的原料,其反应原理是SiO2+2C$\frac{\underline{\;\;△\;\;}}{\;}$ Si+2CO↑(用化学反应方程式表示).
(2)某品牌儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
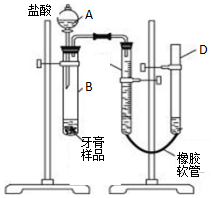
(3)该小组同学拟用如图装置进一步测定某品牌药物牙膏中碳酸钙的含量(牙膏中其它成分遇到C盐酸时无气体生成).试回答下列问题:
①描述实验开始后C、D中的现象:C中液面逐渐降低,D中液面逐渐升高;
②C中所装液体最佳的是c;
a.饱和食盐水 b.蒸馏水c.饱和碳酸氢钠溶液 d.饱和碳酸钠溶液
③B中反应停止后需记录C中液面的读数,读数时应注意:
a.待容器冷却至室温;
b.调节仪器D的高度,使C、D液面相平;
c.读数时视线要平视液面.
④若实验开始所用牙膏样品质量为m g,测得反应产生气体体积为V mL(已经换算为标准状况),则该牙膏样品中碳酸钙的质量分数为$\frac{100V}{224m}%$.
 某研究性学习小组对同学们常用的三种品牌牙膏中摩擦剂成分进行调查,结果如表:
某研究性学习小组对同学们常用的三种品牌牙膏中摩擦剂成分进行调查,结果如表:| 某品牌药物牙膏 | 某品牌儿童牙膏 | 某品牌透明牙膏 | |
| 摩擦剂 | 碳酸钙 | 氢氧化铝 | 二氧化硅 |
(2)某品牌儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
(3)该小组同学拟用如图装置进一步测定某品牌药物牙膏中碳酸钙的含量(牙膏中其它成分遇到C盐酸时无气体生成).试回答下列问题:
①描述实验开始后C、D中的现象:C中液面逐渐降低,D中液面逐渐升高;
②C中所装液体最佳的是c;
a.饱和食盐水 b.蒸馏水c.饱和碳酸氢钠溶液 d.饱和碳酸钠溶液
③B中反应停止后需记录C中液面的读数,读数时应注意:
a.待容器冷却至室温;
b.调节仪器D的高度,使C、D液面相平;
c.读数时视线要平视液面.
④若实验开始所用牙膏样品质量为m g,测得反应产生气体体积为V mL(已经换算为标准状况),则该牙膏样品中碳酸钙的质量分数为$\frac{100V}{224m}%$.
2.下列各组溶液中,可用溴水做试剂将其鉴别出来的是( )
| A. | 汽油、酒精、NaCl溶液 | B. | 汽油、四氯化碳、水 | ||
| C. | 汽油、酒精、NaOH溶液 | D. | 汽油、苯、NaOH溶液 |
9.等物质的量的O2、N2、CO2混合气体通过Na2O2后,体积变为原体积的$\frac{8}{9}$(同温同压),这时混合气体中O2、N2、CO2物质的量之比为( )
| A. | 9:6:0 | B. | 4:3:1 | C. | 3:3:2 | D. | 7:6:3 |
19.下列常见现象与胶体无关的是( )
| A. | 清晨在密林中看到一缕缕的光束 | |
| B. | FeCl3溶液加入NaOH溶液产生红褐色沉淀 | |
| C. | 利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上 | |
| D. | 向豆浆中加入硫酸钙使蛋白质等聚沉,制成可口的豆腐 |
6.下列离子方程式书写正确的是( )
| A. | 稀硫酸与氧化铜反应:O2-+2H+═H2O | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 碳酸钡与盐酸反应:BaCO3+2H+═Ba2++CO2↑+H2O | |
| D. | 向氯化钙溶液中通入CO2:Ca2++H2O+CO2═CaCO3↓+2H+ |
3.据报道,最近苹果公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH- $?_{充电}^{放电}$2CO32-+6H2O,则下列说法正确的是( )
| A. | 构成该电池的正极和负极必须是两种活性不同的金属 | |
| B. | 放电时每消耗1 mol CH3OH转移12 mol电子 | |
| C. | 放电时电解质溶液的pH逐渐增大 | |
| D. | 放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
4.下列离子方程式错误的是( )
| A. | 硅酸钠溶液中通入CO2气体:SiO32-+H2O+CO2═H2SiO3↓+CO32- | |
| B. | 硫酸铝与氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 氯气与氢氧化钾溶液反应:Cl2+OH-═Cl-+ClO-+2H2O | |
| D. | 小苏打溶液与稀盐酸反应:HCO3-+H+═H2O+CO2↑ |