题目内容
12.下列有关电解质溶液说法正确的是( )| A. | pH均为3的溶液,加水稀释10倍后的pH:HCl>H2SO4>CH3COOH | |
| B. | 浓度均为0.1mol•L-1的氨水和氯化铵溶液,水电离出的c(H+)前者小于后者 | |
| C. | 碳酸钠溶液中存在:c(OH-)=c(H+)+c(H2CO3)+c(CO32-) | |
| D. | 0.1mol/L Na2CO3溶液35℃时的碱性比25℃时强,说明盐类水解反应是放热反应 |
分析 A.弱酸在溶液中部分电离,稀释过程中电离程度增大,则醋酸在稀释后溶液的pH最小;
B.氨水中的氢氧根离子抑制了水的电离,氯化铵中铵根离子的水解促进了水的电离;
C.根据碳酸钠溶液中的质子守恒判断;
D.碱性越强,盐的水解程度越大,说明升高温度后碳酸根离子的水解程度增大.
解答 解:A.pH均为3的溶液,盐酸和硫酸都是强酸,稀释过程中氢离子的物质的量基本不变且相等,而醋酸的电离程度增大,稀释后氢离子浓度大于硫酸和盐酸,所以加水稀释10倍后的pH大小为:HCl=H2SO4>CH3COOH,故A错误;
B.浓度均为0.1mol•L-1的氨水和氯化铵溶液,前者抑制了水的电离,而后者促进了水的电离,泽尔水电离出的c(H+)前者小于后者,故B正确;
C.根据碳酸钠溶液中的质子守恒可得:c(OH-)=c(H+)+2c(H2CO3)+c(CO32-),故C错误;
D.0.1mol/L Na2CO3溶液35℃时的碱性比25℃时强,说明升高温度后促进了碳酸根离子的水解,则说明盐类水解反应是吸热反应,故D错误;
故选B.
点评 本题考查了弱电解质的电离平衡、盐的水解原理及其影响,题目难度中等,明确盐的水解原理的影响因素为解答关键,注意掌握弱电解质的电离平衡,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
2.某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种. ①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )

| A. | 溶液中的阳离子有H+、Mg2+、Al3+、NH4+ | |
| B. | 溶液中n(NH4+)=0.2 mol | |
| C. | 溶液中一定不含CO32-和NO3-,可能含有SO42- | |
| D. | n(H+):n(Al3+):n(Mg2+)=2:2:1 |
3.下列各项中实验目的与实验操作和现象相符的是( )
| 选项 | 实验目的 | 实验操作和现象 |
| A | 检验含Fe2+、Fe3+混合溶液中的Fe2+ | 向溶液中加入足量新制氯水,再加入少量KSCN溶液,溶液变红 |
| B | 检验木炭与浓硫酸反应会生成CO2 | 浓硫酸和木炭混合加热,将生成的气体通入足量澄清石灰水,澄清石灰水变浑浊 |
| C | 验证非金属性:Si<C<Cl | 向Na2CO3固体中加入过量盐酸,将产生的气体直接通入NaSiO3中,产生白色沉淀 |
| D | 验证Ksp[Cu(OH)2]<Ksp[Mg (OH)2] | 向NaOH溶液中滴加足量的MgCl2溶液,产生白色沉淀,在滴加足量的CuCl2溶液,沉淀变蓝色 |
| A. | A | B. | B | C. | C | D. | D |
20.利用H2、CH3OH、CO等燃料分别构成燃料电池,它们具有的共同特点是( )
| A. | 正、负极均可为惰性电极 | |
| B. | 正极的电极反应式均为O2+2H20+4e-=40H- | |
| C. | 正极通入的气体必须为纯氧气 | |
| D. | 1mol上述燃料完全放电,转移的电子数均为2mol |
5.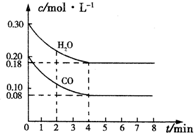 (1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
(1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1,850℃时,此反应的平衡常数为1,CO的转化率为60%.
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
①从表中看出,3~4min之间反应处于平衡状态;c1大于0.08(填“大于”、“小于”或“等于”).
②反应在4~5min间,平衡向逆反应方向移动,可能的原因是c,表中5~6min之间数值发生变化,可能的原因是b.
a.降低温度b.增加水蒸气 c.增加氢气浓度d.使用催化剂.
 (1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
(1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1,850℃时,此反应的平衡常数为1,CO的转化率为60%.
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
| t/min | c(CO)/mol•L-1 | c(H2O)/mol•L-1 | c(CO2)/mol•L-1 | c(H2)/mol•L-1 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4~5min间,平衡向逆反应方向移动,可能的原因是c,表中5~6min之间数值发生变化,可能的原因是b.
a.降低温度b.增加水蒸气 c.增加氢气浓度d.使用催化剂.
12.将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),若经2s后测得C的浓度为0.6mol•L-1,现有下列几种说法正确的是( )
| A. | 2s末用物质A表示的反应速率为0.3mol/(L•s) | |
| B. | 2s内用物质B表示的反应速率为0.15mol/(L•s) | |
| C. | 2s时物质A的转化率为70% | |
| D. | 2s时物质B的浓度为1.4 mol•L-1 |
10.下列各组物质中,所含分子数一定相同的是( )
| A. | 2gH2和16gO2 | |
| B. | 150℃、1.01×105 Pa时,1LCO2和1LH2O | |
| C. | 0.1molHCl和2.24L氩气 | |
| D. | 28gCO和6.02×1022个O3 |