题目内容
12.下列离子反应方程式正确的是( )| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Fe2+与NO3-在酸性溶液中的反应:Fe2++NO3-+4H+=Fe3++NO↑+2H2O | |
| C. | 稀硫酸和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 浓硝酸中加入铜片:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
分析 A.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
B.离子方程式两边总电荷不相等,违反了电荷守恒;
C.氢离子、氢氧根离子的系数错误;
D.铜与浓硝酸反应生成硝酸铜、二氧化氮气体和水.
解答 解:A.氯气溶于水生成氯化氢和次氯酸,次氯酸不能拆开,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故A错误;
B.Fe2+与NO3-在酸性溶液中发生氧化还原反应,反应的离子方程式为:3Fe2++NO3-+8H+=3Fe3++NO↑+4H2O,故B错误;
C.稀硫酸和Ba(OH)2溶液反应生成硫酸钡沉淀和水,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C错误;
D.浓硝酸中加入铜片,反应的离子方程式为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
16.1mol/LH2SO4溶液的含义是( )
| A. | 1L水中含有1mol硫酸 | B. | 1L溶液中含有1molH+ | ||
| C. | 将98gH2SO4溶于1L水所配制的溶液 | D. | 指1L硫酸溶液中含有1molH2SO4 |
3.对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环保、节能减排等目的.汽车尾气脱硝脱碳的主要原理为:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$ N2(g)+2CO2(g)△H=a kJ•mol-1.
I.已知:2NO(g)+O2(g)=2NO2(g)△H=b kJ•mol-1;CO的燃烧热为c kJ•mol-1.写出消除汽车尾气中NO2的污染时,NO2与CO反应的热化学方程式2NO2(g)+4CO(g)=N2(g)+4CO2(g)△H=a-b+2c kJ•mol-1.
II.一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
(1)在恒容密闭容器中充入CO、NO气体,下列图象如图1正确且能说明反应达到平衡状态的是AD.

(2)前2s内的平均反应速率υ(N2)=0.09mol/(L•s)(保留两位小数,下同);此温度下,该反应的平衡常数为0.03mol•L-1.
(3)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液.已知常温下,该溶液的PH=5,则$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=1.7×104(已知该温度下NH3•H2O的Kb=1.7×10-5).若向此溶液中再加入少量 (NH4)2SO4固体,$\frac{c(N{H}_{4}^{+})}{c(S{O}_{4}^{2-})}$的值将变大(填“变大”、“不变”或“变小”).
III.如图2所示,用无摩擦、无质量的活塞1、2将反应器隔成甲、乙两部分,在25℃和101kPa下达到平衡时,各部分体积分别为V甲、V乙.此时若去掉活塞1,不引起活塞2的移动.则x=1.5,V甲:V乙=3:1.
I.已知:2NO(g)+O2(g)=2NO2(g)△H=b kJ•mol-1;CO的燃烧热为c kJ•mol-1.写出消除汽车尾气中NO2的污染时,NO2与CO反应的热化学方程式2NO2(g)+4CO(g)=N2(g)+4CO2(g)△H=a-b+2c kJ•mol-1.
II.一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol•L-1 | 1.00 | 0.8 | 0.64 | 0.55 | 0.5 | 0.5 |
| c(CO)/mol•L-1 | 3.50 | 3.30 | 3.14 | 3.05 | 3.00 | 3.00 |

(2)前2s内的平均反应速率υ(N2)=0.09mol/(L•s)(保留两位小数,下同);此温度下,该反应的平衡常数为0.03mol•L-1.
(3)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO2和NOx,获得(NH4)2SO4的稀溶液.已知常温下,该溶液的PH=5,则$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=1.7×104(已知该温度下NH3•H2O的Kb=1.7×10-5).若向此溶液中再加入少量 (NH4)2SO4固体,$\frac{c(N{H}_{4}^{+})}{c(S{O}_{4}^{2-})}$的值将变大(填“变大”、“不变”或“变小”).
III.如图2所示,用无摩擦、无质量的活塞1、2将反应器隔成甲、乙两部分,在25℃和101kPa下达到平衡时,各部分体积分别为V甲、V乙.此时若去掉活塞1,不引起活塞2的移动.则x=1.5,V甲:V乙=3:1.
7.下列有关Na2CO3溶液中粒子浓度关系不正确的是( )
| A. | c(H+)+c(Na+)>c(CO32-)+c(HCO3-)+c(OH-) | B. | c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-) | ||
| C. | c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | D. | c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
17.下列有关营养成分与人体健康的关系叙述错误的是( )
| A. | 缺铁会患贫血症 | B. | 为防治佝偻病,过量补钙 | ||
| C. | 摄入淀粉量不足,会患低血糖 | D. | 食用蔬菜、水果可以补充维生素 |
4.1molPCl3和2molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g),达平衡时,PCl5为0.4mol,如果此时加入0.5molPCl3和1molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
| A. | 0.6mol | B. | 0.9mol | ||
| C. | 大于0.4mol,小于0.6mol | D. | 大于0.6,小于0.9mol |
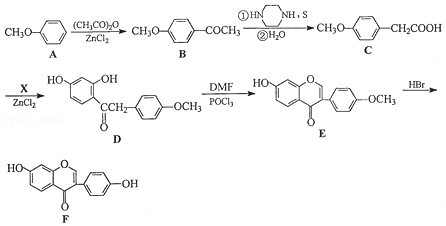
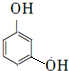 .
.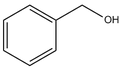 .
.