题目内容
13.下列说法或做法正确的是( )| A. | 正常雨水PH等于7,酸雨的PH小于7 | |
| B. | 金属钠着火燃烧时,可用泡沫灭火器灭火 | |
| C. | 在放电条件下,氮气和氧气化合生成二氧化氮 | |
| D. | 冷的浓硫酸与铁、铝反应时会使金属表面生成致密的氧化物而钝化 |
分析 A.正常的雨水因为溶解了少量的二氧化碳气体而显弱酸性,雨水的pH只是稍小于7,当雨水中溶解了二氧化硫、二氧化氮等物质时,雨水的酸性会明显增强,当达到一定程度时就形成酸雨,pH只是稍小于5.6;
B.Na的性质活泼,易与水反应、与空气中的氧气在点燃或加热时反应生成过氧化钠,过氧化钠能分别与水、二氧化碳反应;
C.放电条件下氮气和氧气反应生成一氧化氮;
D.硫酸具有强氧化性,常温下可使铁、铝钝化.
解答 解:A.正常雨水中因为溶有二氧化碳而显酸性,正常雨水的pH约为5.6,但酸雨的pH却小于5.6,故A错误;
B.金属钠着火时,与空气中的氧气反应生成过氧化钠,过氧化钠与水、二氧化碳反应,而干冰灭火器和泡沫灭火器都生成二氧化碳,只能用干燥沙土盖灭,故B错误;
C.在放电条件下,氮气和氧气化合生成一氧化氮,不能生成二氧化氮,故C错误;
D.浓硫酸具有强氧化性,在常温下可使铁在表面生成一层致密的氧化膜而钝化,故D正确;
故选D.
点评 本题考查酸雨、钠、氮气、浓硫酸的性质,为高考高频考点,侧重于学生的基础知识的综合理解和运用的考查,注意把握浓硫酸的特性以及性质之间的区别,难度不大,注意相关基础的积累.

练习册系列答案
相关题目
4.在反应3BrF3+5H2O=HbrO3+Br2+9HF+O2中,如果有5个水分子发生反应,反应物分子中化合价升高的分子总数和化合价降低的分子总数之比为( )
| A. | 3:1 | B. | 3:2 | C. | 3:5 | D. | 5:3 |
1.将一小块金属钠投入到足量下列物质中,既能生成气体,又能生成白色沉淀的是( )
| A. | MgSO4溶液 | B. | BaCl2溶液 | C. | Fe2(SO4)3溶液 | D. | CuCl2溶液 |
8.下列叙述正确的是( )
| A. | 随着化学科学的发展和提高,自然界的一切都将以人的意志为转移 | |
| B. | 生物固氮是指植物通过叶面直接吸收空气的氮气 | |
| C. | 光导纤维是以二氧化硅为主要原料制成的 | |
| D. | 绿色食品是不含任何化学物质的食品 |
5.能正确表示下列反应的离子方程式的是( )
| A. | 将铜屑加入Fe3+溶液中:2Fe3++Cu═2Fe2++Cu2+ | |
| B. | 碳酸钠水解:CO32-+H2O═HCO3-+OH- | |
| C. | 食醋滴到鸡蛋壳上:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 将铜粉加入稀硫酸中:Cu+2H+═Cu2++H2↑ |
2.在2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl的反应中,氧化剂和还原剂物质的量之比是( )
| A. | 1:8 | B. | 8:1 | C. | 1:5 | D. | 5:1 |
16.根据实验室中测定硫酸铜晶体(CuSO4•XH2O)结晶水含量的实验,填写下列空白:
(1)从下列仪器选出无需用到的仪器是(用标号字母填写)C,E,I.
(A) 电子天平 (B) 坩埚钳 (C) 试管夹 (D) 酒精灯 (E) 蒸发皿
(F) 玻璃棒 (G) 坩埚 (H) 干燥器 (I) 石棉网 (J) 三脚架 (K)泥三角
除上述仪器外,还需要的仪器是研钵、药匙.
(2)某学生实验后得到以下数据:
请写出结晶水含量(H2O%)和X的值的计算公式(用W1、W2、W3表示)
H2O%=44%,X=7.0,该生测定结果是偏高还是偏低?偏高.
(3)从下列分析中选出该学生产生实验误差的原因可能是(填写字母)AB.
(A) 加热过程中晶体有少量溅失;
(B) 加热前称量时容器未完全干燥;
(C) 最后两次加热后的质量相差较大(大于0.1克);
(D) 加热后容器未放入干燥器中冷却;
(4)测定硫酸铜晶体中结晶水的含量,至少在天平上进行四次称量,第三、四次称量的目的是进行恒重操作.
(1)从下列仪器选出无需用到的仪器是(用标号字母填写)C,E,I.
(A) 电子天平 (B) 坩埚钳 (C) 试管夹 (D) 酒精灯 (E) 蒸发皿
(F) 玻璃棒 (G) 坩埚 (H) 干燥器 (I) 石棉网 (J) 三脚架 (K)泥三角
除上述仪器外,还需要的仪器是研钵、药匙.
(2)某学生实验后得到以下数据:
| 加热前质量 | 加热后质量 | |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
| 5.4g | 7.9g | 6.8g |
H2O%=44%,X=7.0,该生测定结果是偏高还是偏低?偏高.
(3)从下列分析中选出该学生产生实验误差的原因可能是(填写字母)AB.
(A) 加热过程中晶体有少量溅失;
(B) 加热前称量时容器未完全干燥;
(C) 最后两次加热后的质量相差较大(大于0.1克);
(D) 加热后容器未放入干燥器中冷却;
(4)测定硫酸铜晶体中结晶水的含量,至少在天平上进行四次称量,第三、四次称量的目的是进行恒重操作.
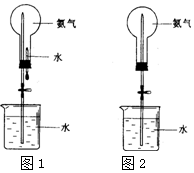 喷泉是一种常见的自然现象,其产生的原因是存在压强差.制取氨气并完成喷泉实验(图中夹持装置均已略去).
喷泉是一种常见的自然现象,其产生的原因是存在压强差.制取氨气并完成喷泉实验(图中夹持装置均已略去).