题目内容
X、Y、Z为三种单质,常温下X为金属,Y是液体,Z是无色气体.其反应关系如图所示,其中B的溶液显强酸性.请回答下列问题:
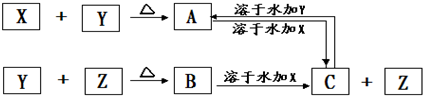
(1)根据上述关系,确定X、Z的化学式:X 、Z ;
(2)Y元素在周期表中的位置是 ;
(3)写出A溶于水后加X的离子方程式: ;
(4)写出C溶液中通入过量氯气的离子方程式: .

(1)根据上述关系,确定X、Z的化学式:X
(2)Y元素在周期表中的位置是
(3)写出A溶于水后加X的离子方程式:
(4)写出C溶液中通入过量氯气的离子方程式:
考点:无机物的推断
专题:推断题
分析:X、Y、Z为三种单质,Z是无色气体,Y+Z=B,B的溶液显强酸性,可考虑B可能是卤族元素的氢化物;X、Y、Z为三种单质,X为金属,Y是液体,Y为溴;Z是无色气体,只能是氢气,氮气,氧气,因能和溴反应,故为氢气;X为金属,其溴化物和X单质本身能反应,故有变价,X为铁,据此解答.
解答:
解:X、Y、Z为三种单质,Z是无色气体,Y+Z=B,B的溶液显强酸性,可考虑B可能是卤族元素的氢化物;X、Y、Z为三种单质,X为金属,Y是液体,Y为Br2;Z是无色气体,只能是氢气,氮气,氧气,因能和溴反应,故Z为H2;X为金属,其溴化物和X单质本身能反应,故有变价,X为铁,
(1)由上分析知X、Z的化学式分别为Fe、H2 ,故答案为:Fe;H2;
(2)Y为溴元素,位于第四周期第ⅦA族,故答案为:第四周期第ⅦA族;
(3)A溶于水后加X即FeBr3溶于水后加Fe的离子方程式2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)FeBr2溶液中通入过量氯气,则Fe2+和Br-均被氧化,对应离子方程式为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故答案为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-.
(1)由上分析知X、Z的化学式分别为Fe、H2 ,故答案为:Fe;H2;
(2)Y为溴元素,位于第四周期第ⅦA族,故答案为:第四周期第ⅦA族;
(3)A溶于水后加X即FeBr3溶于水后加Fe的离子方程式2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)FeBr2溶液中通入过量氯气,则Fe2+和Br-均被氧化,对应离子方程式为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-,故答案为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-.
点评:本题考查了Fe3+和Fe2+的互相转化、卤族元素的性质、元素周期表等知识,均属于基础知识,平时应注意加强识记即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
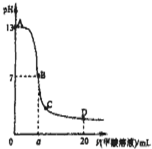 向15mL 0.1mol?L-1KOH溶液中逐滴加入0.2mol?L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确的是( )
向15mL 0.1mol?L-1KOH溶液中逐滴加入0.2mol?L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确的是( )| A、在A、B间任意一点c(K+)>c(HCOO-)>c(OH-)>c(H+) |
| B、在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 |
| C、在C点:c(HCOO-)>c(K+)>c(OH-)>c(H+) |
| D、在D点:c(HCOO-)+c(HCOOH)>2c(K+) |
在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是( )
| A、CH4和C2H4 |
| B、C2H2和C2H4 |
| C、C2H4和C2H6 |
| D、C3H4和C3H6 |
化学与生活息息相关.下列叙述错误的是( )
| A、明矾溶液可以对自来水进行净水 |
| B、电解法精炼粗铜,纯铜做阴极 |
| C、铅蓄电池的负极是Pb |
| D、增大压强平衡一定发生移动 |
下列各组反应中最终肯定不生成白色沉淀的是( )
| A、AlCl3溶液中加入过量氨水 |
| B、Al2(SO4)3溶液中加入过量KOH溶液 |
| C、MgCl2溶液中加入过量氢氧化钠 |
| D、澄清石灰水中通入过量CO2 |
氢氧燃料电池是一种新能源.如图为氢氧燃料电池示意图.下列说法不正确的是( )
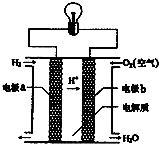

| A、a极是正极,b极是负极 |
| B、该装置能将化学能转化为电能 |
| C、电子由a极通过导线流向b极 |
| D、供电时总反应为2H2+O2=2H2O |
氧化镁、碳酸氢钠、氢氧化铝、碳酸钙均可用于治疗胃酸(主要成分是盐酸)过多.它们分别与盐酸反应,依次对应的离子方程式正确的是( )
| A、MgO+2H+=Mg2++H2O |
| B、CO32-+2H+=CO2↑+H2O |
| C、OH-+H+=H2O |
| D、CaCO3+H+=Ca2++CO2↑+H2O |