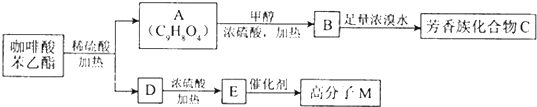
题目内容
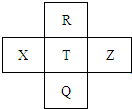 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中只有X是短周期的金属元素,下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中只有X是短周期的金属元素,下列判断正确的是( )| A、X的最高价氧化物能溶于强碱 |
| B、非金属性:T<R |
| C、气态氢化物稳定性:T>Z |
| D、R与Q的原子核外电子数相差16 |
考点:原子结构与元素的性质
专题:
分析:元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中只有X是短周期的金属元素,则X为Al元素,R为C元素,T为Si元素,Q为Ge元素,Z为P元素,结合元素周期律解答.
解答:
解:A.X为Al元素,氧化铝能溶于强碱,故A正确;
B.同主族从上到下非金属性依次减弱,则非金属性:T<R,故B正确;
C.同周期从左到右非金属性依次增强,对应气态氢化物的稳定性依次增强,则气态氢化物稳定性:T<Z,故C错误;
D.R为C元素,Q为Ge元素,二者原子核外电子数相差26,故D错误.
故选AB.
B.同主族从上到下非金属性依次减弱,则非金属性:T<R,故B正确;
C.同周期从左到右非金属性依次增强,对应气态氢化物的稳定性依次增强,则气态氢化物稳定性:T<Z,故C错误;
D.R为C元素,Q为Ge元素,二者原子核外电子数相差26,故D错误.
故选AB.
点评:本题考查结构位置性质关系、元素周期表的结构、元素周期律等,难度不大,推断X为Al元素是解题的关键,注意掌握元素周期律.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在室温时,下列各组物质分别与一定量NaOH溶液反应,在溶液中可能生成6种酸根离子的是( )
| A、A12O3、SO2、CO2、SO3 |
| B、C12、A12O3、N2O5、SO3 |
| C、CO2、C12、CaO、SO3 |
| D、SiO2、N2O5、CO、C12 |
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式.以下用于研究有机物的方法中正确的是( )
| A、重结晶法一般适用于被提纯的有机物在溶剂中的溶解度受温度影响较大的混合物的分离 |
| B、对有机物分子红外光谱图的研究有助于确定有机物相对分子质量 |
| C、燃烧法是确定有机物分子官能团的有效方法 |
| D、质谱法通常用于分析确定有机物分子的元素组成 |
用石墨作电极,电解下列物质的溶液,其实质不是电解水的是( )
| A、NaNO3 |
| B、NaOH |
| C、Na2SO4 |
| D、NaCl |
下列离子方程式正确的是( )
| A、铁粉和氯化铁溶液反应 Fe+Fe3+═Fe2+ |
| B、铁和稀盐酸反应 Fe+2H+═Fe2++H2↑ |
| C、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| D、铝和氢氧化钠溶液反应 2Al+2OH-=2AlO2-+3H2↑ |
下列有机物命名正确的是( )
| A、2,3,3-三甲基丁烷 |
| B、2-乙基戊烷 |
| C、3-乙基-1-戊烯 |
| D、2,2-二甲基-1-丁烯 |
 近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )
近年来,科学家合成了一种稳定的氢铝化合物Al2H6.Al2H6的球棍模型如图所示,它的熔点为150℃,可用作高能燃料或储氢材料.下列说法正确的是( )| A、60g Al2H6中含铝原子约为1.2×1023个 |
| B、1mol Al2H6中约含有4.8×1024个σ键 |
| C、Al2H6可以燃烧,产物为氧化铝和水 |
| D、Al2H6在固态时所形成的晶体是离子晶体 |
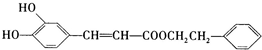 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: