题目内容
20.用NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 2g氢气所含原子数目为NA | |
| B. | 1.7g NH3中含N-H键数目为0.1NA | |
| C. | 标准状况下,22.4L单质溴所含有的原子数目为2NA | |
| D. | 1molMg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
分析 A、氢气由氢原子构成;
B、求出氨气的物质的量,然后根据氨气中含3条N-H键来分析;
C、标况下溴为液态;
D、镁反应后变为+2价.
解答 解:A、氢气由氢原子构成,故2g氢气中含有的氢原子的物质的量为2mol,个数为2NA个,故A错误;
B、1.7g氨气的物质的量为0.1mol,而氨气中含3条N-H键,故0.1mol氨气中含0.3NA个N-H键,故B错误;
C、标况下溴为液态,故不能根据气体摩尔体积来计算其物质的量和含有的原子个数,故C错误;
D、镁反应后变为+2价,故1mol镁反应后失去2mol电子即2NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案
相关题目
10. 在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | Y是电源的正极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2ˉ,CO2+2e-═CO+O2- | |
| C. | 总反应可表示为:H2+CO2═H2+CO | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
11.某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M,经测定Fe3+、SO42-、Al3+和M的物质的量之比为2:4:1:1,则M可能是下列中的( )
| A. | Na+ | B. | OH- | C. | Cl- | D. | S2- |
8.“优化结构、提高效益和降低消耗、保护环境”,这是我国国民经济和社会发展的基础性要求.你认为下列行为不符合这个要求的是( )
| A. | 将煤转化成气体燃料可以有效地减少“温室效应”的气体产生 | |
| B. | 加快太阳能、风能、生物质能、海洋能等清洁能源的开发利用 | |
| C. | 研制开发以水代替有机溶剂的化工涂料 | |
| D. | 大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
15.短周期主族元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为18.X与Y、Z位于相邻周期,Y原子最外层电子数是X原子内层电子数的3倍,下列说法正确的是( )
| A. | Y的低价氧化物能使Z单质的水溶液褪色 | |
| B. | X的氢化物溶于水显酸性 | |
| C. | 其离子半径大小:Z>Y>X | |
| D. | X的氢化物和Z的最高价氧化物对应的水化物不能反应生成盐 |
12.化学与人类生产、生活密切相关,下列说法正确的是( )
| A. | 有机玻璃受热软化,易于加工成型,是一种硅酸盐材料 | |
| B. | 煤的气化是物理变化,是高效、清洁地利用煤的重要途径 | |
| C. | 纯银器在空气中久置变黑是因为发生了电化学腐蚀 | |
| D. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 |
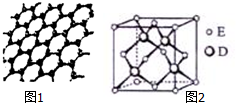 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族且相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族且相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: