题目内容
2.下列说法符合化学事实的是( )| A. | 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 | |
| B. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 | |
| C. | Na2SiO3水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| D. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 |
分析 A.油脂为高级脂肪酸甘油酯;
B.硅胶、石灰均作干燥剂,铁粉作抗氧化剂;
C.Na2SiO3水溶液俗称水玻璃,不燃烧,具有防腐作用;
D.氯水中含HClO,具有漂白性.
解答 解:A.油脂为高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油,故A错误;
B.硅胶、石灰均作干燥剂,铁粉作抗氧化剂,作用不同,故B错误;
C.Na2SiO3水溶液俗称水玻璃,不燃烧,具有防腐作用,与二氧化碳反应生成硅酸,则是制备硅胶和木材防火剂的原料,故C正确;
D.氯水中含HClO,具有漂白性,不能利用pH试纸测pH,应选pH计测定,故D错误;
故选C.
点评 本题考查物质的组成、结构与性质,为高频考点,把握物质的性质、应用及化学与生活的关系为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
12.某均匀混合的白色粉末可能含有下列7种常见物质中的某4种:NaCl、BaCl2、Mg(NO3)2、K2CO3、CuSO4、NaHCO3、X,混合物中各成分的物质的量相等,且所含阴、阳离子数目之比为3:2,某同学做了以下实验,部分现象没有描述.根据所提供的实验现象,下列对该白色粉末的判断正确的是( )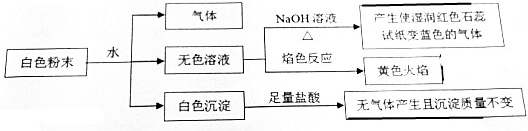

| A. | 一定含有BaCl2、Mg(NO3)2、NaHCO3、X,且X是NH4HSO4 | |
| B. | 一定不含K2CO3、CuSO4,X是NH4Al(SO4)2 | |
| C. | 一定含有BaCl2、NaHCO3、X且X是NH4AlO2,另一种为NaCl和Mg(NO3)2中的任一种 | |
| D. | 一定含有NaCl、BaCl2、NaHCO3和X,当X不能确定是什么物质 |
13.某溶液中可能含有物质的量浓度相等的下列离子中的几种:Fe3+、Cu2+、Na+、SO42-、CO32-、NO3-、Cl-、I-,取上述溶液少量分别进行如下实验:
①一份中加入少量锌粉后,固体溶解、溶液颜色有变化,但无其它现象产生
②一份加入BaCl2溶液后得到白色沉淀,下列有关判断正确的是( )
①一份中加入少量锌粉后,固体溶解、溶液颜色有变化,但无其它现象产生
②一份加入BaCl2溶液后得到白色沉淀,下列有关判断正确的是( )
| A. | 溶液中只含Fe3+、SO42-、Cl- | |
| B. | 溶液中只含Cu2+、SO42- | |
| C. | 需要利用焰色反应才能确定有无Na+ | |
| D. | 溶液中肯定没有I-,但无法确定有无Cl- |
7.下列有关叙述正确的是( )
| A. | 银锌纽扣电池工作时,Ag2O被还原为Ag | |
| B. | 碱性锌锰电池中,MnO2是催化剂 | |
| C. | 放电时,铅酸蓄电池中硫酸浓度不断增大 | |
| D. | 电镀时,待镀的金属制品表面发生还原反应 |
12.已知某烃A相对氢气的密度为42,且该烃不能使溴的CCl4溶液褪色.则A的可能结构共有(不考虑立体异构)( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
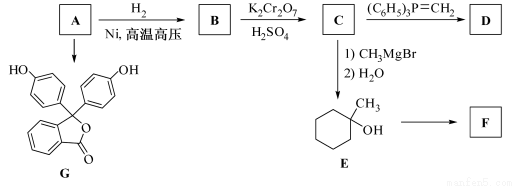
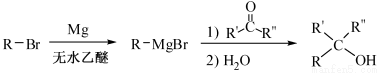
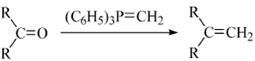 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢) 、
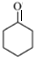
、
 或
或 (任写一种)
(任写一种)
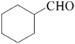 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: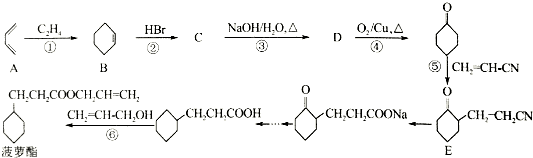
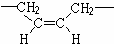 ,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.
,若顺丁橡胶的平均相对分子质量为540054,则平均聚合度为10001.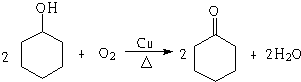 .
.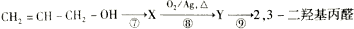
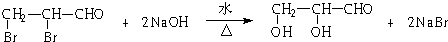 .
.