题目内容
下列图示与对应的叙述不相符的是
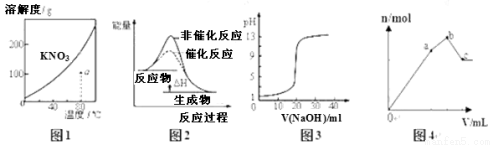
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
C
【解析】
试题分析:A.KNO3的溶解度随温度的升高而增大,所以图1表示KNO3的溶解度曲线,图中a点所示的溶液由于溶质没有达到该温度的最大溶解的质量,因此是80℃时KNO3的不饱和溶液,正确;B.催化剂能够改变反应途径,降低反应的活化能,但是不能改变反应热,因此图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化,正确;C.用0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液,若二者的体积相等,得到的是醋酸钠是强碱弱酸盐,水解使溶液嫌你碱性,而图示显示的是酸性,与实际不符合,错误;D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,先发生反应:Al2(SO4)3+ 3Ba(OH)2=BaSO4↓+2Al(OH)3↓,接着发生反应:(NH4) 2SO4+ Ba(OH)2=BaSO4↓+NH3?H2O,当该反映完全,又发生反应:2Al(OH)3+ Ba(OH)2=Ba(AlO2)2+4H2O,沉淀的质量又有所减小。与图像吻合,正确。
考点:考查图像法在表示物质的溶解度与温度的关系、化学反应历程、酸碱中和滴定及沉淀的物质的量与加入物质是多少的关系的应用的知识。

(7分)实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。请完成下列填空:
取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验 编号 | NaOH溶液的浓度 (mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 22.50 | 20.00 |
2 | 0.10 | 25.80 | 20.00 |
3 | 0.10 | 22.62 | 20.00 |
(1)滴定达到终点的标志是 。
(2)根据上述数据,可计算出该盐酸的浓度约为______________(保留两位有效数字)。
(3)排去碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
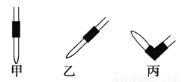
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______(填选项字母)。
A.滴定终点读数时俯视
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
 O2(g)===CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1 O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1 CH3OH(g) ΔH=________kJ·mol-1
CH3OH(g) ΔH=________kJ·mol-1

 2C(s)+2D(g),5 min后反应达到平衡,测得生成C为0.8 mol,下列相关表述正确的是
2C(s)+2D(g),5 min后反应达到平衡,测得生成C为0.8 mol,下列相关表述正确的是