题目内容
11.标准状态下,672mL某气体质量为0.84g,该气体摩尔质量为28g/mol.分析 依据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$计算解答.
解答 解:标准状态下,672ml某气体物质的量=$\frac{0.672L}{22.4L/mol}$=0.03mol,摩尔质量=$\frac{0.84g}{0.03mol}$=28g/mol;
故答案为:28g/mol.
点评 本题考查物质的量有关计算、微粒数目计算,明确基本公式是解本题关键,注意对基础知识的理解掌握,题目难度不大.

练习册系列答案
相关题目
19.下列对部分化学知识的归纳完全正确的一组是( )
| A. |
| |||||
| B. |
| |||||
| C. |
| |||||
| D. |
|
6. 用图所示装置进行下列各组实验,具体操作如下:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列各组实验,具体操作如下:将①中溶液滴入②中,预测的现象与实际相符的是( )
 用图所示装置进行下列各组实验,具体操作如下:将①中溶液滴入②中,预测的现象与实际相符的是( )
用图所示装置进行下列各组实验,具体操作如下:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测的实验现象 |
| A | 浓盐酸 | 二氧化锰固体 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生白色沉淀 |
| D | 稀硫酸 | 滴有石蕊的亚硫酸钠溶液 | 溶液逐渐变红 |
| A. | A | B. | B | C. | C | D. | D |
16.工业制硝酸时,NH3在500℃时可以发生如下3个反应,下列说法正确的是( )
| 反应 | △H(kJ•mol-1) | 平衡常数K |
| ①4NH3(g)+5O2(g)?4NO(g)+6H2O(g) | -907 | 1.1×1026 |
| ②4NH3(g)+4O2(g)?2N2O(g)+6H2O(g) | -1105 | 4.4×1028 |
| ③4NH3(g)+3O2(g)?2N2 (g)+6H2O(g) | -1269 | 7.1×1034 |
| A. | N2(g)+O2(g)=2NO(g)△H=362 kJ•mol-1 | |
| B. | 增大压强,则反应②的K 不变,反应①和③的K 减小 | |
| C. | 500℃,2N2O(g)+O2(g)?4 NO(g) K=4×102 | |
| D. | 使用合适的催化剂可提高反应的选择性,提高NO 的产出率 |
20.取四个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4:1)的混合气体、二氧化氮和氧气(体积比为4:3)的混合气体;然后分别做溶解于水的喷泉实验.实验结束后四个烧瓶中所得溶液的物质的量浓度之比为( )
| A. | 2:1:2:2 | B. | 5:5:5:4 | C. | 5:5:4:4 | D. | 7:7:4:3 |
1.下列有关物质的用途不正确的是( )
| A. | 液氨可用作制冷剂 | B. | SO2广泛用于食品漂白 | ||
| C. | 铁制容器可用于存储浓硝酸 | D. | 浓硫酸不能用来干燥氨气 |
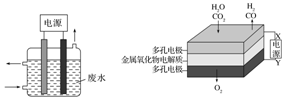 用图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O;
用图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,阳极的电极反应式为:Cl-+2OH--2e-═ClO-+H2O; 实验室可用氯酸钾与密度为1.19g•cm-3,溶质质量分数为36.5%的浓盐酸反应制取氯气.
实验室可用氯酸钾与密度为1.19g•cm-3,溶质质量分数为36.5%的浓盐酸反应制取氯气.