题目内容
5.将一定质量的KOH和Ca(OH)2混合物全部溶于一定量水中形成稀溶液,再缓缓通入CO2气体.生成沉淀的质量随通入CO2的体积(标准状况下)变化如图所示,试计算(1)混合物中Ca(OH)2的质量为0.74g
(2)所配得溶液中,KOH的物质的量为0.02mol.

分析 (1)得到沉淀为CaCO3,其质量最大为1.0g,根据钙元素守恒n[Ca(OH)2]=n(CaCO3),再根据m=nM计算混合物中Ca(OH)2的质量;
(2)通入896mL二氧化碳时,沉淀又完全溶解,此时溶液中溶质为Ca(HCO3)2、KHCO3,根据Ca元素守恒计算n[Ca(HCO3)2],再根据碳元素守恒计算n(KHCO3),由钾原子守恒可得n(KOH)=n(KHCO3).
解答 解:(1)得到沉淀为CaCO3,其质量最大为1.0g,根据钙元素守恒n[Ca(OH)2]=n(CaCO3)=$\frac{1.0g}{100g/mol}$=0.01mol,故混合物中Ca(OH)2的质量为0.01mol×74g/mol=0.74g,
故答案为:0.74;
(2)通入896mL二氧化碳时,沉淀又完全溶解,此时溶液中溶质为Ca(HCO3)2、KHCO3,根据Ca元素守恒n[Ca(HCO3)2]=n[Ca(OH)2]=0.01mol,再根据碳元素守恒n(KHCO3)=n(CO2)-2n[Ca(HCO3)2]=
$\frac{0.896L}{22.4L/mol}$-2×0.01mol=0.02mol,由钾原子守恒可得n(KOH)=n(KHCO3)=0.02mol,
故答案为:0.02.
点评 本题考查混合物计算,题目利用守恒法解答,避免过程的繁琐,侧重考查学生分析计算能力,难度中等.

练习册系列答案
相关题目
15.在c(NH4+)=0.1mol•L-1的NH4Fe(SO4)2溶液中,下列各组离子能大量共存的是( )
| A. | H+、Ba2+、Br-、I- | B. | K+、Na+、CO32-、OH- | ||
| C. | Cu2+、Al3+、Cl-、NO3- | D. | Ca2+、Mg2+、CH3COO-、SCN- |
16.下列说法不正确的是 ( )
| A. | 含0.1mol H2SO4的浓硫酸与含0.2 mol NaOH的溶液混合,放出的热量即为中和热 | |
| B. | 化学键断裂时吸收能量,形成时放出能量 | |
| C. | 增大反应物的浓度,可增加单位体积内活化分子数,从而使反应速率增大 | |
| D. | 为了防止轮船的钢铁外壳被腐蚀,可以在外壳上连接锌块 |
13.下列选项中,表示ⅥA族某元素原子结构示意图的是( )
| A. | 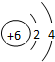 | B. | 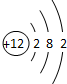 | C. | 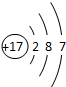 | D. | 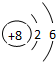 |
20.下列说法正确的是( )
| A. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| B. | 淀粉和蛋白质水解的最终产物都能发生银镜反应 | |
| C. | 油脂都是高级脂肪酸甘油酯,在碱性条件下能发生皂化反应 | |
| D. | “乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物 |
10.下列物质在空气中久置会发生变质,且在变质过程中,既有氧化还原反应发生,又有非氧化还原反应发生的是( )
| A. | 氢氧化钠固体 | B. | 氯化钠固体 | C. | 金属钠 | D. | 生石灰 |
17.下列各组离子,在强酸性溶液中能大量共存的是( )
| A. | Na+、K+、Ca2+、HCO3- | B. | NO3-、Cl-、Na+、Ag+ | ||
| C. | Cu2+、Fe2+、SO42-、Cl- | D. | Mg2+、Na+、Cl-、CH3COO- |
14.下列化学用语表述正确的是( )
| A. | 甲烷的球棍模型: | B. | 氯化氢的电子式: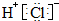 | ||
| C. | Cl2的结构式:Cl=Cl | D. | 硫离子的结构示意图: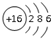 |
15.鸡舍中常不断地产生氨气.在大规模养鸡场中,氨气常引发鸡群出现呼吸道疾病,甚至会造成鸡的大批死亡.下列物质不适合于吸收氨气的是( )
| A. | 硫酸溶液 | B. | 醋酸溶液 | C. | Na0H固体 | D. | 硝酸溶液 |