题目内容
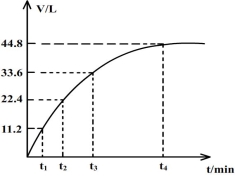
向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L。若将该混合物加入500mL14 mol·L-1的HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体?(假设浓度小于9mol/L为稀HNO3)( )
A. t1B.t2C.t3D.t4
C
【解析】
试题分析:设Al、Fe的物质的量分别是x、ymol,则27x+56y=44.4,二者与过量盐酸反应生成氢气的物质的量是26.88L/22.4L/mol=1.2mol,所以3/2x+y=1.2,两式联立可解x=0.4mol,y=0.6mol。该混合物与500mL14mol/L的硝酸反应生成气体的物质的量是44.8L/22.4L/mol=2mol,设生成的NO2、NO的物质的量分别是m、nmol, m+n=2mol,若铁反应的产物是+3价铁离子,则消耗的硝酸最多,被还原的硝酸的物质的量是2mol,未被还原的硝酸的物质的量是0.4mol×3+0.6mol×3=3.0mol,则共消耗硝酸的物质的量是3+2=5mol<0.5L×14mol/L=7mol,所以铁应生成+3价铁离子,根据电荷守恒可得0.4×3+0.6mol×3=m+3n,解得m=1.5mol,n=0.5mol,即理论上生成的二氧化氮标准状况下的体积是33.6L,NO的体积是11.2L,所以在t3时刻开始产生NO,答案选C。
考点:考查金属与酸的反应及氧化还原反应的计算,守恒法的应用

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目