题目内容
15.BaSO4的分子量为233,Ksp=1.0×10-10,把1.0mmol的BaSO4配成10dm3溶液,BaSO4没有溶解的量是( )| A. | 0.0021g | B. | 0.021g | C. | 0.21g | D. | 2.1g |
分析 依据硫酸钡的Ksp计算饱和溶液中钡离子的浓度,把1.0mmol的BaSO4配成10dm3溶液,依据溶液体积和浓度计算10dm3 饱和溶液中钡离子物质的量,计算BaSO4没有溶解的量;
解答 解:Ksp=c(Ba2+)c(SO42-)=1.0×10-10,可知钡离子在饱和溶液中浓度为c(Ba2+)=1.0×10-5mol/L,把1.0mmol的BaSO4配成10dm3溶液,10dm3=1L,1.0mmol=1.0×10-3mol,饱和溶液中溶解的钡离子物质的量=1.0×10-5mol/L×10dm3=1.0×10-4mol,计算得BaSO4没有溶解的量是1.0×10-3×mol/L×233g/mol-1.0×10-4mol×233g/mol=0.21g,
故选C.
点评 本题考查了沉淀溶解平衡的分析,溶度积常数和离子浓度的计算,注意饱和溶液中溶解物质的量的计算,题目难度中等.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
17.除去下列物质中的少量杂质(括号内),选用的试剂和分离方法不能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 粗苯甲酸(泥沙等) | 水 | 重结晶 |
| B | 甲烷(乙烯) | 高锰酸钾酸性溶液 | 洗气 |
| C | 乙炔(硫化氢) | 硫酸铜溶液 | 洗气 |
| D | 溴苯(溴) | 稀氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
3.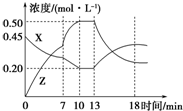 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
 向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )
向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+Y(g)?2Z(g)△H<0.如图所示是容器中X、Z的物质的量浓度随时间变化的曲线.下列关于在第7min 时和第13min时曲线变化的可能原因推测正确的是( )| A. | 第7 min时升高温度、第13 min时降低温度 | |
| B. | 第7 min时使用催化剂、第13 min时升高温度 | |
| C. | 第7 min时降低温度、第13 min时增大压强 | |
| D. | 第7 min时减小压强、第13 min时升高温度 |
20.下列化学反应可以设计成原电池的是( )
| A. | 2H2+O2═2H2O | B. | H++OH-═H2O | ||
| C. | .CaCO3═CaO+CO2↑ | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
4.在甲乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-六种离子中的三种,已知乙烧杯中的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )
| A. | Cu2+、H+、Cl- | B. | Cl-、CO32-、OH- | C. | K+、OH-、CO32- | D. | K+、H+、Cl- |


