题目内容
A~G及X、Y均是中学化学常见物质,其中B、D、E、F、G在常温下为气体且B为红棕色,F的水溶液呈碱性,C为金属单质,A、X分别为其对应的氧化物和盐,X的溶液为蓝色,它们之间有如下转化关系(部分反应产物已略去).

(1)F分子的电子式为 .
(2)按照要求写出下列变化的化学用语:
①X的水溶液呈弱酸性,请用离子方程式表示其原因: .
②电解X溶液的阳极反应式 .
③写出反应Ⅶ的离子方程式 .
(3)将充满气体B的玻璃球浸泡在冰水中,气体颜色 .
(4)若使F按下列途径完全转化为Y,则参加反应的F与整个过程中消耗D的物质的量之比为 .


(1)F分子的电子式为
(2)按照要求写出下列变化的化学用语:
①X的水溶液呈弱酸性,请用离子方程式表示其原因:
②电解X溶液的阳极反应式
③写出反应Ⅶ的离子方程式
(3)将充满气体B的玻璃球浸泡在冰水中,气体颜色
(4)若使F按下列途径完全转化为Y,则参加反应的F与整个过程中消耗D的物质的量之比为

考点:无机物的推断
专题:推断题
分析:A~G及X、Y均是中学化学常见物质,B、D、E、F、G在常温下为气体,F的水溶液呈碱性,则F为NH3,B为红棕色,则B为NO2,溶于水得到Y与E,则Y为HNO3、E为NO,G与D在放电条件下得到E,G、D分别为N2、O2中的一种,E能与D进一步反应得到B,故D为O2、G为N2,C为金属单质,A、X分别为其对应的氧化物和盐,X的溶液为蓝色,可推知C为Cu,A为CuO,Cu与Y(硝酸)浓溶液反应得到X,可推知X为Cu(NO3)2,据此解答.
解答:
解:A~G及X、Y均是中学化学常见物质,B、D、E、F、G在常温下为气体,F的水溶液呈碱性,则F为NH3,B为红棕色,则B为NO2,溶于水得到Y与E,则Y为HNO3、E为NO,G与D在放电体积下得到E,G、D分别为N2、O2中的一种,E能与D进一步反应得到B,故D为O2、G为N2,C为金属单质,A、X分别为其对应的氧化物和盐,X的溶液为蓝色,可推知C为Cu,A为CuO,Cu与Y(硝酸)浓溶液反应得到X,可推知X为Cu(NO3)2,
(1)由上述分析可知,F为NH3,其电子式为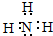 ,故答案为:
,故答案为: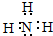 ;
;
(2)①X为Cu(NO3)2,水溶液中Cu2+水解:Cu2++2H2O?Cu(OH)2+2H+,破坏水的电离平衡,呈弱酸性,
故答案为:Cu2++2H2O?Cu(OH)2+2H+;
②电解Cu(NO3)2溶液,阳极上水放电得到氧气与氢离子,阳极电极反应式为:2H2O-4e-=O2↑+2 H+,
故答案为:2H2O-4e-=O2↑+2 H+;
③反应Ⅶ的离子方程式为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,
故答案为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(3)存在平衡2NO2?N2O4,正反应为放热反应,充满气体NO2的玻璃球浸泡在冰水中,平衡正向移动,气体颜色变浅,
故答案为:变浅;
(4)整个过程为NH3最终得到HNO3,N元素化合价由-3升高为+5,氧气中氧元素化合价由0价降低为-2,根据电子转移守恒可知,[5-(-3)]n(NH3)=4n(O2),故n(NH3):n(O2)=1:2,
故答案为:1:2.
(1)由上述分析可知,F为NH3,其电子式为
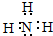 ,故答案为:
,故答案为: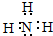 ;
;(2)①X为Cu(NO3)2,水溶液中Cu2+水解:Cu2++2H2O?Cu(OH)2+2H+,破坏水的电离平衡,呈弱酸性,
故答案为:Cu2++2H2O?Cu(OH)2+2H+;
②电解Cu(NO3)2溶液,阳极上水放电得到氧气与氢离子,阳极电极反应式为:2H2O-4e-=O2↑+2 H+,
故答案为:2H2O-4e-=O2↑+2 H+;
③反应Ⅶ的离子方程式为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,
故答案为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(3)存在平衡2NO2?N2O4,正反应为放热反应,充满气体NO2的玻璃球浸泡在冰水中,平衡正向移动,气体颜色变浅,
故答案为:变浅;
(4)整个过程为NH3最终得到HNO3,N元素化合价由-3升高为+5,氧气中氧元素化合价由0价降低为-2,根据电子转移守恒可知,[5-(-3)]n(NH3)=4n(O2),故n(NH3):n(O2)=1:2,
故答案为:1:2.
点评:本题考查无机物推断,物质的状态、颜色、F的水溶液呈碱性及转化关系中特殊反应等是推断突破口,需要学生熟练掌握元素化合物性质、电解原理等,难度中等.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
X、Y、Z是周期表中相邻的三种短周期元素,它们原子半径依次减小,X与Z的核电荷数之比为3:4,X、Y、Z分别与氢元素形成氢化物.下列叙述正确的是( )
| A、Z是第二周期ⅣA族元素 |
| B、最高价氧化物对应的水化物的酸性:Y<X |
| C、非金属性:X<Y<Z |
| D、X、Y、Z的氢化物稳定性逐渐减弱 |
 氯气常用于自来水厂杀菌消毒.
氯气常用于自来水厂杀菌消毒.



 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: