题目内容
工业上常常会大量的废料,如果不加以回收利用甚至会造成环境污染,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜 的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。

请回答:
(1)写出步骤Ⅰ反应的离子方程式:_________________________。
(2)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是____________。
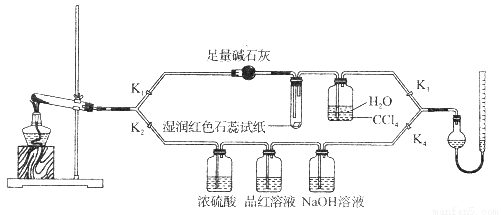
(3)进行步骤Ⅱ时,该小组用如图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察 到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是____________________。
到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是____________________。

(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径②中反应的离子方程式:__________________________,
请选出你认为的最佳途径并说明选择的理由:______________________________。
 阅读快车系列答案
阅读快车系列答案| 选项 | 实验操作和现象 | 实验结论 |
| A | 常温下,将大小、形状形态的锌和铝分别加入到等体积98%的浓硫酸中,观察到前者反应速率快 | 锌比铝活泼 |
| B | 向某溶液中加入盐酸酸化的氯化钡溶液,产生白色沉淀 | 该溶液中一定含有SO42- |
| C | 将盐酸滴入碳酸钠溶液中,产生气泡 | 非金属性:Cl大于C |
| D | 向某溶液中加入氢氧化钡溶液丙加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定含有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
分部分中学化学常见元素原子结构及性质如表所示:
序号 | 元素 | 结构及性质 |
① | A | A是一种常见金属,它的一种氧化物是具有磁性的黑色晶体 |
② | B | B是一种常见金属,原子核外有三个电子层且最外层电子为偶数 |
③ | C | C的气态氢化物易液化常作制冷剂 |
④ | D | D为灰黑色具有金属光泽的固体,是太阳能电池板的常用材料 |
⑤ | E | E原子最外层电子数是内层电子总数的3倍 |
⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A原子在周期表中的位置为______________,离子半径:B2+_________C3-(填"大于、小于或等于”)。
(2)简单气态氢化物的热稳定性:D__________E(填"大于、小于或等于”)。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是________________。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的电子式为__________,N的结构式为___________。
(4)用化学方程式表明C与E这两种元素的非金属性的强弱_________________。
| A. | 原混合物中铜和铁各0.065mol | |
| B. | 稀硝酸的物质的量浓度为4.0mol•L-1 | |
| C. | 第一次剩余的4.8g金属为铜和铁 | |
| D. | 向反应后的溶液中再加入该稀硝酸100mL,又得到NO在标准状况下的体积为0.56 L |


 H溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是
H溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是