题目内容
NA代表阿伏加德罗常数,下列说法错误的是( )
| A、标准状况下,22.4L NO和22.4L O2的混合,混合气体中含有的氧原子数为3NA | ||||
| B、0.012kg 13C中,含中子数为7NA | ||||
| C、25℃时,1L pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子 | ||||
D、在反应3SiO2+6C+2N2
|
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据化学反应实质是原子的重新组合,原子守恒分析判断;
B、依据n=
计算物质的量,结合质量数=质子数+中子数计算分析;
C、依据PH和离子积常数计算氢氧根离子浓度,结合n=
=CV计算;
D、依据化学方程式中元素化合价变化分析计算电子转移;
B、依据n=
| m |
| M |
C、依据PH和离子积常数计算氢氧根离子浓度,结合n=
| N |
| NA |
D、依据化学方程式中元素化合价变化分析计算电子转移;
解答:
解:A、在22.4 L NO中有1 mol氧原子、22.4 L O2 2 mol氧原子,依据原子守恒分析化学反应不改变原子数,A项正确;
B、0.012 kg 13C不是1 mol,含中子数小于7NA,故B项错误;
C、pH=13,c(H+)=0.1 mol/L,n(H+)=1 L×0.1 mol/L=0.1 mol,C项正确;
D、在反应中6个C失去12个电子,2N2得到12个电子,生成1 mol Si3N4时共转移12 NA电子,D项正确;
故选B.
B、0.012 kg 13C不是1 mol,含中子数小于7NA,故B项错误;
C、pH=13,c(H+)=0.1 mol/L,n(H+)=1 L×0.1 mol/L=0.1 mol,C项正确;
D、在反应中6个C失去12个电子,2N2得到12个电子,生成1 mol Si3N4时共转移12 NA电子,D项正确;
故选B.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是反应实质理解,氧化还原反应电子转移计算应用,电解质溶液中离子积计算判断,掌握基础是关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 常温下,向20mL 0.1mol/L酒石酸(用H2T表示)溶液中逐滴滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系.下列说法正确的是( )
常温下,向20mL 0.1mol/L酒石酸(用H2T表示)溶液中逐滴滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系.下列说法正确的是( )| A、VNaOH=10mL时,溶液中存在[Na+]=2[H2T]+2[HT-]+2[T2-] |
| B、VNaOH=20mL时,溶液中存在[Na+]>[HT-]>[H+]>[H2T]>[T2-] |
| C、VNaOH=30mL时,溶液中存在[Na+]>[HT-]>[T2-]>[OH-]>[H+] |
| D、VNaOH=40mL时,溶液中存在[OH-]=[HT-]+2[H2T]+[H+] |
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、46g乙醇中含有的化学键数为7NA |
| B、1mol氯气和足量NaOH溶液反应转移电子数为2NA |
| C、1mol OH-和1mol-OH(羟基)中含有的质子数均为9NA |
| D、10L 0.1mol?L-1的Na2CO3溶液中,Na+、CO32-总数为3NA |
甲、乙、丙、丁4种无机化合物均含有2种元素,分子中均含18个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
| A、某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B、乙和甲中同种元素的质量分数相等,则乙能使湿润的KI淀粉试纸变蓝 |
| C、丙中含有ⅣA族元素,则相同条件下丙比甲稳定 |
| D、若丁的分子组成符合XY3型结构,则丁分子间存在氢键 |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、NO3- | ||
B、常温下,
| ||
| C、滴入酚酞试液显红色的溶液:Mg2+、Al3+、Br-、SO42- | ||
| D、能溶解Al2O3的溶液:Na+、Ca2+、HCO3-、NO3- |
 碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题:
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.请回答下列问题: 用如图所示装置进行实验,实验现象正确的是( )
用如图所示装置进行实验,实验现象正确的是( )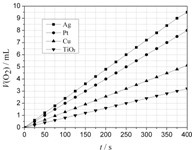 某些金属及金属氧化物对H2O2的分解反应具有催化作用,请回答下列问题:
某些金属及金属氧化物对H2O2的分解反应具有催化作用,请回答下列问题: