题目内容
11.下列化学用语表述正确的是( )| A. | 羟基的电子式: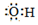 | B. | 聚丙烯的结构简式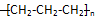 | ||
| C. | 四氯化碳分子的电子式 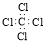 | D. | 丙烷分子的球棍模型 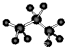 |
分析 A.羟基含有9个电子;
B.聚丙烯是丙烯中双键其中的1个键断裂发生自身加聚反应,链节主链含有2个C原子;
C.漏写Cl的核外电子;
D.球棍模型突出的是原子之间的成键的情况及空间结构.
解答 解:A.羟基是电中性基团,氧原子与氢原子以1对共用电子对连接,电子式为 ,故A错误;
,故A错误;
B.聚丙烯是丙烯中双键其中的1个键断裂发生自身加聚反应,链节主链含有2个C原子,聚丙烯结构简式为 ,故B错误;
,故B错误;
C.四氯化碳的电子式为: ,故C错误;
,故C错误;
D. 原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,故D正确.
原子之间为单键,主链有3个碳原子,氢原子数为8个,符合丙烷的结构,故D正确.
故选D.
点评 本题考查化学用语的使用,为高频考点,侧重考查学生双基知识,注意把握常见化学用语的书写规范,难度不大,易错选项是C,书写共价化合物电子式易漏掉孤电子对,为易错点.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
1.在一密闭容器中有一氧化碳、甲醛、氢气、氧气的混合气体共23.6g,加入足量Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增加10.8g,则原混合气体中氧气的物质的量是( )
| A. | 0.4 mol | B. | 0.34 mol | C. | 0.8 mol | D. | 0.74 mol |
19.19世纪末,开始揭开原子内部的秘密,最早发现电子的科学家是( )
| A. | 英国的道尔顿 | B. | 英国的卢瑟福 | C. | 丹麦的玻尔 | D. | 英国的汤姆生 |
16.柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是( )
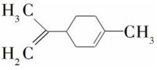

| A. | 柠檬烯的一氯代物有7种 | |
| B. | 柠檬烯和丁基苯互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | 在一定条件下,柠檬烯可以发生加成、取代、氧化、还原等反应 |
3.元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语.下列有关化学用语的表示方法中错误的是( )
| A. | 次氯酸的电子式: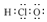 | B. | S2-的结构示意图: | ||
| C. | O-18的原子符号:${\;}_{\;}^{15}$O | D. | CO2分子的结构式:O=C=O |
20.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气体 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 元素B的单质可被热的浓硫酸或浓硝酸氧化 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
1.X、Y、Z是3种原子序数逐渐增大的短周期元素,其中X、Y位于同一主族,X原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )
| A. | 元素非金属性由弱到强的顺序为Z<Y<X | |
| B. | 化合物YZ2中各原子都达到8电子结构 | |
| C. | 这3种元素的氢化物的沸点由高到低的顺序为:Z>Y>X | |
| D. | 其对应的阴离子半径由大到小的顺序为:Z>Y>X |