题目内容
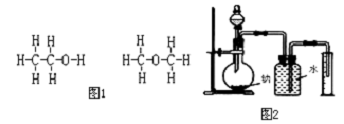
经元素质量分析测得乙醇的分子式是C2H6O.由于有机化合物普遍存在同分异构现象,根据价键理论,推测乙醇结构可能是图1两种之一:
为确定其结构,应利用物质的特殊性质进行定性、定量实验.现给出乙醇、钠、水等药品及必要的仪器,用如图2所示的装置进行实验确定乙醇的结构.某学生得到一组实验数据:
(1)根据以上数据推断乙醇的结构应为 ,理由 (用化学方程式表示).
(2)写出工业上以乙稀为原料制取乙醇的化学方程式 .
(3)图2装置用来测量产生氢气的体积是否有误差? (答“有”或“无”)
为确定其结构,应利用物质的特殊性质进行定性、定量实验.现给出乙醇、钠、水等药品及必要的仪器,用如图2所示的装置进行实验确定乙醇的结构.某学生得到一组实验数据:
| 乙醇的用量(物质的量) | 产生氢气的体积(标准状况) |
| 0.10mol | 1.12L |
(2)写出工业上以乙稀为原料制取乙醇的化学方程式
(3)图2装置用来测量产生氢气的体积是否有误差?

考点:乙醇与金属钠的反应
专题:
分析:(1)根据乙醇能和金属钠反应生成氢气来推测乙醇中含有醇羟基;
(2)工业上以乙稀和水反应生成乙醇;
(3)图2装置用来测量产生氢气的体积有误差,真正的原因是广口瓶与量筒之间玻璃导管中水柱的体积没计算在内.
(2)工业上以乙稀和水反应生成乙醇;
(3)图2装置用来测量产生氢气的体积有误差,真正的原因是广口瓶与量筒之间玻璃导管中水柱的体积没计算在内.
解答:
解:(1)实验数据表明:0.1mol C2H6O与足量的钠反应,产生1.12L H2,即0.05mol H2,也就是0.1mol H.说明1个C2H6O分子中只有1个氢原子被Na置换,故结构式为 ,反应的化学方程式为2C2H5OH+2Na-→2C2H5ONa+H2↑;
,反应的化学方程式为2C2H5OH+2Na-→2C2H5ONa+H2↑;
故答案为: ;2C2H5OH+2Na-→2C2H5ONa+H2↑;
;2C2H5OH+2Na-→2C2H5ONa+H2↑;
(2)工业上以乙稀和水反应生成乙醇,化学方程式为 ;
;
故答案为: ;
;
(3)图2装置用来测量产生氢气的体积有误差,真正的原因是广口瓶与量筒之间玻璃导管中水柱的体积没计算在内,故答案为:有.
 ,反应的化学方程式为2C2H5OH+2Na-→2C2H5ONa+H2↑;
,反应的化学方程式为2C2H5OH+2Na-→2C2H5ONa+H2↑;故答案为:
 ;2C2H5OH+2Na-→2C2H5ONa+H2↑;
;2C2H5OH+2Na-→2C2H5ONa+H2↑; (2)工业上以乙稀和水反应生成乙醇,化学方程式为
 ;
;故答案为:
 ;
;(3)图2装置用来测量产生氢气的体积有误差,真正的原因是广口瓶与量筒之间玻璃导管中水柱的体积没计算在内,故答案为:有.
点评:本题考查学生实验设计能力,测量气体体积的方法及分析误差的能力,是一个探究性实验,难度较大.

练习册系列答案
相关题目
采用下列装置和操作,不能达到实验目的是( )


| A、甲装置:在乙醇与乙酸的混合液中加入足量生石灰,可蒸馏出乙醇 |
| B、乙装置:用CCl4萃取溴水中的溴,并把溴的CCl4溶液从下口放出 |
| C、丙装置:广口瓶中盛酸性高锰酸钾溶液,除去CH4中的少量SO2 |
| D、丁装置:A中为乙醇、醋酸,B为饱和碳酸钠溶液,制取乙酸乙酯 |
下列物质互为同分异构体的是( )
| A、1H、D、T |
| B、C60和C70 |
| C、乙酸和甲酸甲酯 |
| D、CH3OC2H5和CH3CH2OCH3 |
如图是两种兴奋剂的结构简式:

关于它们的说法中正确的是( )

关于它们的说法中正确的是( )
| A、1mol X与足量的NaOH溶液在常温常压下反应,最多消耗3mol NaOH |
| B、1mol X与足量的氢气反应,最多消耗2mol H2 |
| C、Y与足量的浓溴水反应,能产生白色沉淀 |
| D、Y遇到FeCl3溶液时显紫色,但不能使溴的四氯化碳溶液褪色 |


 ,请写出实验室保存该有机物方法:
,请写出实验室保存该有机物方法: X、Y、Z、W、Q均为短周期元素,其中Y、Z、W、Q在元素周期表中的相对位置如图,X是周期表中半径最小的元素,Q的原子序数是W的2倍.
X、Y、Z、W、Q均为短周期元素,其中Y、Z、W、Q在元素周期表中的相对位置如图,X是周期表中半径最小的元素,Q的原子序数是W的2倍.