题目内容
乙酸是食醋的主要成分.
(1)乙酸的分子式是 ;(2)乙酸可使紫色石蕊溶液变 色;
(3)一定条件下,乙酸能与乙醇发生反应生成一种具有香味的油状液体.某研究性学习小组成员分别设计了如图甲、乙、丙三套实验装置:
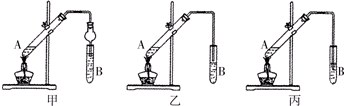
①B试管中的液体物质是 ,A中发生反应的化学方程式为 ,该有机反应的类型是 反应.
②甲、乙、丙三套装置中,不宜选用的装置是 (填“甲”、“乙”、“丙”)
③试管B中的液体能和生成物中混有的某杂质发生反应,该反应的化学方程式是 .
(1)乙酸的分子式是
(3)一定条件下,乙酸能与乙醇发生反应生成一种具有香味的油状液体.某研究性学习小组成员分别设计了如图甲、乙、丙三套实验装置:

①B试管中的液体物质是
②甲、乙、丙三套装置中,不宜选用的装置是
③试管B中的液体能和生成物中混有的某杂质发生反应,该反应的化学方程式是
考点:乙酸乙酯的制取,乙酸的化学性质
专题:有机物的化学性质及推断
分析:(1)乙酸分子式为C2H4O2,
(2)乙酸含官能团羧基,乙酸为弱酸,具有酸的通性;
(3)①饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
乙酸能与乙酸发生反应生成乙酸乙酯,为酯化反应,也属于取代反应.
②吸收极易溶于水的气体时,若将导管伸入水中,由于气体溶于水,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象;
③乙酸乙酯中混有乙酸可和碳酸钠反应.
(2)乙酸含官能团羧基,乙酸为弱酸,具有酸的通性;
(3)①饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
乙酸能与乙酸发生反应生成乙酸乙酯,为酯化反应,也属于取代反应.
②吸收极易溶于水的气体时,若将导管伸入水中,由于气体溶于水,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象;
③乙酸乙酯中混有乙酸可和碳酸钠反应.
解答:
解:(1)乙酸分子式为C2H4O2,故答案为:C2H4O2;
(2)乙酸含官能团羧基,乙酸为弱酸,具有酸的通性,可使紫色石蕊变红;
故答案为:红;
(3)①制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯;所以B试管中盛放的溶液是饱和碳酸钠溶液;乙酸能与乙酸发生反应生成乙酸乙酯,该反应为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,为酯化反应,也属于取代反应,
故答案为:饱和碳酸钠溶液;CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;酯化(或取代);
②甲、乙、丙三套装置中,甲装置中,导管伸入吸收液中,并且连接了体积较大的容器,既能够防止倒吸,又能够很好的吸收乙酸乙酯中的乙酸和乙醇,乙装置中,将导管伸入液面上,能够很好的吸收乙酸乙酯中的乙酸和乙醇,可防止倒吸,丙装置中将导管伸入饱和碳酸钠溶液中,由于乙酸和乙醇溶于饱和碳酸钠溶液,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象,
故答案为:丙;
③乙酸乙酯中混有乙酸和碳酸钠发生复分解反应,反应方程式为:Na2CO3+2CH3COOH=2CH3COONa+CO2↑+2H2O 故答案为:Na2CO3+2CH3COOH=2CH3COONa+CO2↑+2H2O.
(2)乙酸含官能团羧基,乙酸为弱酸,具有酸的通性,可使紫色石蕊变红;
故答案为:红;
(3)①制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯;所以B试管中盛放的溶液是饱和碳酸钠溶液;乙酸能与乙酸发生反应生成乙酸乙酯,该反应为CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:饱和碳酸钠溶液;CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
②甲、乙、丙三套装置中,甲装置中,导管伸入吸收液中,并且连接了体积较大的容器,既能够防止倒吸,又能够很好的吸收乙酸乙酯中的乙酸和乙醇,乙装置中,将导管伸入液面上,能够很好的吸收乙酸乙酯中的乙酸和乙醇,可防止倒吸,丙装置中将导管伸入饱和碳酸钠溶液中,由于乙酸和乙醇溶于饱和碳酸钠溶液,导致装置内压强急剧降低,外界大气压压着液体进入,产生倒吸现象,
故答案为:丙;
③乙酸乙酯中混有乙酸和碳酸钠发生复分解反应,反应方程式为:Na2CO3+2CH3COOH=2CH3COONa+CO2↑+2H2O 故答案为:Na2CO3+2CH3COOH=2CH3COONa+CO2↑+2H2O.
点评:本题考查乙酸乙酯的制备,解答时须注意饱和碳酸钠溶液的作用,题目难度不大.

练习册系列答案
相关题目
下列有关电解质溶液的说法不正确的是( )
| A、升高温度,水的电离平衡常数增大 |
| B、1mol/L的NaHCO3溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=1mol/L |
| C、常温时,饱和AgCl溶液与饱和AgI溶液相比,前者的c(Ag+)大 |
| D、在醋酸溶液中加入少量醋酸钠固体,能促进醋酸的电离 |
将乙酸(其中的氧都18O标记)在浓硫酸存在条件下与足量的乙醇充分反应.下叙述不正确的是( )
| A、生成是水分子中含有18O |
| B、生成的乙酸乙酯相对分子质量为88 |
| C、生成的乙酸乙酯的相对分子质量为90 |
| D、此反应是有限度的 |
下列有关元素非金属性的比较,正确的是( )
| A、进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 | ||
| B、HCl溶液的酸性比H2S溶液的酸性强,则Cl的非金属性比S强 | ||
C、2C+SiO2
| ||
| D、测定NaCl和NaF溶液的pH,可确定F、Cl两元素非金属性的强弱 |
 可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空:
可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空: