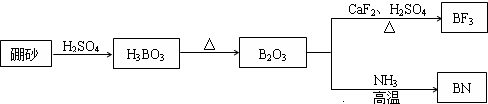
题目内容
在HF、H2O、NH3、CS2、CH4、N2分子中:
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,具有三角锥型结构的极性分子是
(5)以极性键相结合,具有V型结构的极性分子是 .
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,具有三角锥型结构的极性分子是
(5)以极性键相结合,具有V型结构的极性分子是
考点:极性键和非极性键,极性分子和非极性分子
专题:化学键与晶体结构
分析:由不同种非金属元素形成的化学键为极性键,由同种非金属元素形成的化学键为非极性键,
结构对称,正负电荷的中心重合,则为非极性分子;
结构不对称,正负电荷的中心不重合,为极性分子以此来解答.
结构对称,正负电荷的中心重合,则为非极性分子;
结构不对称,正负电荷的中心不重合,为极性分子以此来解答.
解答:
解:HF中含有H-F极性键,直线型结构,正负电荷的中心不重合,为极性分子;
H2O中含有H-O极性键,空间构型为V型,正负电荷的中心不重合,为极性分子;
NH3 中含有N-H极性键,分子为三角锥构型,结构不对称,正负电荷的中心不重合,为极性分子;
CS2含有C=S极性键,分子为线型结构,结构对称,正负电荷的中心重合,为非极性分子;
CH4含有C-H极性键,分子为正四面体结构,结构对称,正负电荷的中心重合,为非极性分子;
N2含有N≡N极性键,结构对称,正负电荷的中心重合,为非极性分子;
故答案为:(1)N2 (2)CS2 (3)CH4 (4)NH3 (5)H2O.
H2O中含有H-O极性键,空间构型为V型,正负电荷的中心不重合,为极性分子;
NH3 中含有N-H极性键,分子为三角锥构型,结构不对称,正负电荷的中心不重合,为极性分子;
CS2含有C=S极性键,分子为线型结构,结构对称,正负电荷的中心重合,为非极性分子;
CH4含有C-H极性键,分子为正四面体结构,结构对称,正负电荷的中心重合,为非极性分子;
N2含有N≡N极性键,结构对称,正负电荷的中心重合,为非极性分子;
故答案为:(1)N2 (2)CS2 (3)CH4 (4)NH3 (5)H2O.
点评:本题考查极性键和非极性键,极性分子和非极性分子,分子的空间构型,题目难度不大,判断键的极性关键抓住成键原子是否是同种元素原子;判断分子的极性关键在于明确分子的结构,正负电荷中心是否重合.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、95℃纯水的pH<7,说明加热可导致水呈酸性 |
| B、常温下,将pH=3的醋酸溶液稀释至10倍后溶液pH=4 |
| C、常温下,将0.2 mol?L-1的盐酸与等体积水混合后溶液pH=1 |
| D、常温下,将pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合后溶液pH<7 |
在下列反应中,HCl 既体现酸性又体现还原性的是( )
| A、NaOH+HCl=NaCl+H2O | ||||
| B、Zn+2HCl=ZnCl2+H2↑ | ||||
C、MnO2+4HCl(浓)
| ||||
| D、CuO+2HCl=CuCl2+H2O |
下列图示与对应的叙述相符的是( )
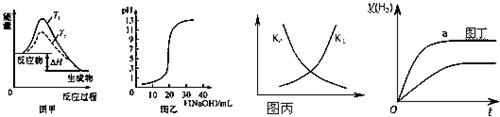

| A、图甲表示温度T1>T2,SO2与O2反应过程中的能量变化 |
| B、图乙表示0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L CH3COOH溶液所得到的滴定曲线 |
| C、图丙表示恒容密闭容器中反应“2SO2(g)+O2(g)?2SO3(g)△H<0”的平衡常数K正、K逆随温度的变化 |
| D、图丁表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |