题目内容
2.下列化学用语表达正确的是( )| A. | NaHCO3的电离方程式:NaHCO3═Na++H++CO32- | |
| B. | CaCO3的沉淀溶解平衡表达式:CaCO3(s)?Ca2+(aq)+CO32-(aq) | |
| C. | NaHS发生水解的离子方程式:HS-+H2O?S2-+H3O+ | |
| D. | 碳酸的电离方程式:H2CO3?2H++CO32- |
分析 A.碳酸氢根为弱酸的酸式根离子,不能拆;
B.碳酸钙部分溶解出钙离子、碳酸根离子;
C.硫氢根离子水解生成硫化氢和氢氧根离子;
D.碳酸为多元弱酸,分步电离,以第一步为主.
解答 解:A.NaHCO3的电离方程式:NaHCO3═Na++HCO3-,故A错误;
B.CaCO3的沉淀溶解平衡表达式:CaCO3(s)?Ca2+(aq)+CO32-(aq),故B正确;
C.NaHS发生水解的离子方程式:HS-+H2O?H2S+OH-,故C错误;
D.碳酸的电离方程式:H2CO3?H++HCO3-,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,涉及电解质电离方程式、盐类水解的离子方程式书写,明确反应实质,盐类水解规律、电解质强弱及电离方式是解题关键,题目难度不大.

练习册系列答案
相关题目
12.在下列各溶液中离子一定能大量共存的是( )
| A. | 强碱溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 含0.1mol?L-1Fe3+的溶液中:K+、Ba2+、NO3-、SO42- | |
| C. | 含0.1mol?L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 室温下c(H+)=0.1mol?L-1的溶液中:Na+、Fe3+、NO3-、SO42- |
13.有K2SO4、Al2(SO4)3的混合溶液,已知其中的Al3+、SO42-的浓度分别为0.4mol/L、0.7mol/L,则该溶液中K+的物质的量浓度为( )
| A. | 0.1mol/L | B. | 0.15mol/L | C. | 0.2mol/L | D. | 0.25mol/L |
7.已知钴(Co)的相对原子质量为59,一种钴的氧化物含+2价钴24.48%,+3价钴48.96%,则该钴的氧化物的化学式为( )
| A. | Co2O3 | B. | Co3O3 | C. | Co3O4 | D. | Co5O7 |
2.100mL 6mol•L-1 H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A. | Na2CO3(s) | B. | 水 | C. | 硝酸钾溶液 | D. | 盐酸 |
3.青蒿酸是合成青蒿素的原料,可以由香草醛合成:
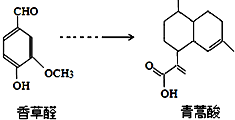
下列叙述正确的是( )

下列叙述正确的是( )
| A. | 青蒿酸分子中含有4个手性碳原子 | |
| B. | 在一定条件,香草醛可与HCHO发生缩聚反应 | |
| C. | 两种物质分别和H2反应,最多消耗H24mol和3mol | |
| D. | 可用FeCl3溶液或NaHCO3溶液鉴别化合物香草醛和青蒿酸 |
 、
、 、
、 或
或 .
.