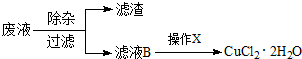
题目内容
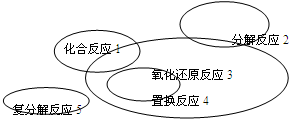
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于3区域的是 (3区域为除去1、2、4交叉部分)( )

| A、Cl2+2KBr═Br2+2KCl | ||||
B、CaCO3
| ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、2CuO+2CO
|
考点:化学基本反应类型
专题:物质的性质和变化专题
分析:由图可知,区域3的反应不属于化合反应,不属于分解反应,不属于置换反应,但一定属于氧化还原反应,以此来解答.
解答:
解:A.Cl2+2KBr═Br2+2KCl属于置换反应,不符合,故A不选;
B.CaCO3
CaO+CO2↑属于分解反应,不符合,故B不选;
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3属于化合反应,不符合,故C不选;
D.2CuO+2CO
2Cu+2CO2不属于化合反应,不属于分解反应,不是置换反应,属于氧化还原反应,符合,故D选;
故选D.
B.CaCO3
| ||
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3属于化合反应,不符合,故C不选;
D.2CuO+2CO
| ||
故选D.
点评:本题考查基本反应类型与氧化还原反应的关系,难度不大.明确区域3表示的反应是解答本题的关键,熟悉基本反应类型及氧化还原反应的判断即可解答.

练习册系列答案
相关题目
下列基本实验操作中,正确的是( )
A、 气体除杂 |
B、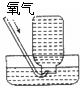 收集氧气 |
C、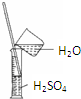 稀释溶液 |
D、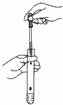 稀释溶液 |
下列离子方程式不正确的是( )
| A、向Ba(OH)2溶液中滴加NH4HSO4溶液刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
| B、向Ca(HCO3)2溶液中加入少量Ca(OH)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、在NaOH溶液中通入少量的SO2气体:SO2+OH-=HSO3- |
| D、二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O |
根据组成特点和所具有的性质,通常把无机物分为单质、氧化物、酸、碱、盐.某物质溶于水,所得溶液既能使蓝色石蕊试纸变红,也能与碳酸盐反应生成气体,此物质有可能是( )
①单质 ②氧化物 ③酸 ④碱 ⑤盐.
①单质 ②氧化物 ③酸 ④碱 ⑤盐.
| A、①②③⑤ | B、①②④ |
| C、②③④ | D、①②③④⑤ |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1mol N2所含有的原子数为NA |
| B、标准状况下,22.4L水中含有的水分子数为NA |
| C、78g Na2O2与足量水充分反应时电子转移数为2NA |
| D、32g O2所含的氧原子数目为2NA |
下列溶液中微粒浓度关系一定正确的是( )
| A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)>c(H+) |
| C、0.1mol?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、0.1mol?L-1的硫化钠溶液中:c(OH-)=c(H+)>c(HS-)>c(H2S) |
 短周期元素X、Y、Z的位置如图所示,已知Y、Z两元素原子序数之和是X原子序数的4倍.X、Y、Z三元素的元素符号是( )
短周期元素X、Y、Z的位置如图所示,已知Y、Z两元素原子序数之和是X原子序数的4倍.X、Y、Z三元素的元素符号是( )| A、N、Si、S |
| B、O、P、C1 |
| C、F、S、Ar |
| D、C、A1、P |
下列图示的实验能达到实验目的是( )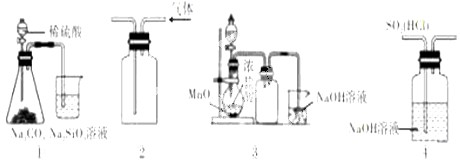

| A、图①实验装置可验证非金属性:S>C>Si |
| B、图②实验装置收集NO2气体 |
| C、图③实验装置可制备、收集Cl2 |
| D、图③实验装置可去除SO2中HCl |