题目内容
在一定条件下某反应的热化学方程式为:2SO2(g)+O2(g)?2SO3(g);△H=-197kJ/mol
现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如表所示.根据以下数据,下列叙述正确的是( )
现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如表所示.根据以下数据,下列叙述正确的是( )
| 容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A、Q2=98.5 kJ |
| B、2SO2(g)+O2(g)?2SO3(s);△H>-197KJ/mol |
| C、丙容器中压强大于乙,所以丙的反应速率大于乙 |
| D、2Q3<Q1<197KJ |
考点:化学平衡的计算
专题:
分析:A、根据热化学方程式及可逆反应的特点判断;
B、根据物质在不同状态变化中的热量变化判断;
C、根据影响反应速率 的因素判断;
D、根据平衡的移动及可逆反应中的反应热进行判断.
B、根据物质在不同状态变化中的热量变化判断;
C、根据影响反应速率 的因素判断;
D、根据平衡的移动及可逆反应中的反应热进行判断.
解答:
解:A、根据热化学方程式2SO2(g)+O2(g)?2SO3(g);△H=-197kJ/mol,1molSO2完全反应可放出98.5 kJ的热,在容器乙中,1molSO2不可能完全反应,所以Q2<98.5 kJ,故A错误;
B、SO3固体变为气体要吸热,△H<-197KJ/mol,故B错误;
C、丙容器中压强大于乙,是因为有氮气的存在,氮气不参加反应,而丙和乙各反应物的浓度相同,所以氮气对反应速率没有影响,所以两容器中反应速率相等,故C错误;
D、由于反应2SO2(g)+O2(g)?2SO3(g)是可逆反应,所以Q1<197KJ,在丙容器中,反应浓度为甲容器的一半,氮气对平衡没有影响,相当于平衡时甲基、容器的压强大于丙容器,所以平衡时丙容器反应正向进行的程度小于甲容器,所以2Q3<Q1,故D正确;
故选D.
B、SO3固体变为气体要吸热,△H<-197KJ/mol,故B错误;
C、丙容器中压强大于乙,是因为有氮气的存在,氮气不参加反应,而丙和乙各反应物的浓度相同,所以氮气对反应速率没有影响,所以两容器中反应速率相等,故C错误;
D、由于反应2SO2(g)+O2(g)?2SO3(g)是可逆反应,所以Q1<197KJ,在丙容器中,反应浓度为甲容器的一半,氮气对平衡没有影响,相当于平衡时甲基、容器的压强大于丙容器,所以平衡时丙容器反应正向进行的程度小于甲容器,所以2Q3<Q1,故D正确;
故选D.
点评:本题主要考查可逆反应中的热量的变化情况,题目难度中等,本题注意浓度对平衡的影响以及可逆反应的特征.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验操作中,用于分离食用油和氯化钠溶液的最佳方案是( )
A、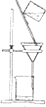 |
B、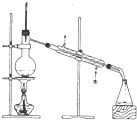 |
C、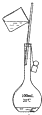 |
D、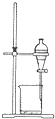 |
可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
| A、分别加入碘水,观察颜色反应 |
| B、分别加热,观察是否生成沉淀 |
| C、加入淀粉酶观察是否水解 |
| D、分别灼烧,闻味道 |
为减少新鲜蔬菜中的维生素C的流失,下列有关烹调蔬菜的方法不妥当的是( )
| A、蔬菜最好洗干净后再切 |
| B、炒蔬菜的时间不能太长,炒熟即可 |
| C、新鲜蔬菜应放在冰箱中储存 |
| D、把蔬菜放在高压锅中焖煮 |
下列物质中,不能和氯气发生取代反应的是( )
| A、C8H18 |
| B、C2H5Cl |
| C、CH2Cl2 |
| D、CCl4 |
下列说法正确的是( )
| A、过量的铁在氯气中燃烧可生成氯化亚铁 |
| B、向Fe(NO3)2溶液加入盐酸,由于酸性增强抑制Fe2+的水解,使c(Fe2+)增大 |
| C、Fe和Fe2O3的混合物溶于盐酸中,再加入KSCN溶液,溶液一定变为血红色 |
| D、把一定量的铁和铜的混和粉未投入到FeCl3溶液中,不可能出现只有铁剩余没有铜剩余的情况 |
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、K+、MnO4-、Na+、Cl- |
| B、Na+、H+、NO3-、SO42- |
| C、Fe3+、Na+、Cl-、SO42- |
| D、K+、Na+、NO3-、CO32- |
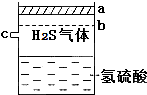 已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.
已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度…在密闭容器里盛有饱和H2S溶液和H2S气体,可上下移动的活塞停止在a处,如图所示.