题目内容
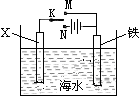 已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用如图装置进行实验探究,下列说法正确的是( )
已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用如图装置进行实验探究,下列说法正确的是( )| A、X为锌棒,K置于M,可减缓铁的腐蚀,铁电极上发生的反应为2H++2e-=H2↑ |
| B、X为锌棒,K置于M,外电路电流方向是从X到铁 |
| C、X为碳棒,K置于N,可减缓铁的腐蚀,利用的是外加电流的阴极保护法 |
| D、X为碳棒,K置于N,在X电极周围首先失电子的是Cl- |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:X为锌棒,K置于M,形成原电池,锌较活泼,应为负极,铁为正极;X为碳棒,K置于N,为电解装置,X为阳极,铁为阴极,阳极上还原性强的阴离子先失电子,结合原电池和电解池的工作原理解答该题.
解答:
解:A.X为锌棒,K置于M,形成原电池,电解质溶液呈中性,发生吸氧腐蚀,铁电极上发生的反应为O2+4e-+2H2O=4OH-,故A错误;
B.X为锌棒,K置于M,形成原电池,锌较活泼,应为负极,铁为正极,外电路电流方向是从铁到X,故B错误;
C.X为碳棒,K置于N,为电解装置,铁为阴极,电源提供电子,铁被保护,难以腐蚀,为外加电流的阴极保护法,故C正确;
D.X为碳棒,K置于N,X为阳极,阳极上还原性强的先失电子,则在X电极周围首先失电子的是Br-,故D错误.
故选C.
B.X为锌棒,K置于M,形成原电池,锌较活泼,应为负极,铁为正极,外电路电流方向是从铁到X,故B错误;
C.X为碳棒,K置于N,为电解装置,铁为阴极,电源提供电子,铁被保护,难以腐蚀,为外加电流的阴极保护法,故C正确;
D.X为碳棒,K置于N,X为阳极,阳极上还原性强的先失电子,则在X电极周围首先失电子的是Br-,故D错误.
故选C.
点评:本题综合考查原电池和电解池知识,侧重于电化学原理和金属的腐蚀与防护知识,题目难度不大,注意把握电极方程式的书写.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
a1和a2分别为A在两个恒容容器中平衡体系A(g)?2B(g) 和2A(g)?B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是( )
| A、a1、a2均减小 |
| B、a1、a2均增大 |
| C、a1增大,a2减小 |
| D、a1减小,a2增大 |
NaCl是一种化工原料,可以制备一系列物质(如图).下列说法正确的是( )
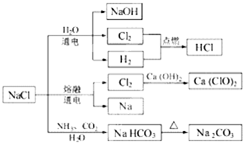

| A、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B、石灰乳与Cl2的反应中,Cl2是氧化剂,Ca(OH)2是还原剂 |
| C、常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D、如图所示转化反应中有4个反应属于氧化还原反应 |
化学与社会、环境密切相关,下列有关说法正确的是( )
| A、绿色化学的核心是应用化学原理对环境污染进行治理 |
| B、氯气和氢氧化钠溶液和石灰乳得到的含氯化合物都具有漂白性 |
| C、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
| D、对“地沟油”蒸馏可以获得汽油 |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、X与Y形成化合物,X可以显负价,Y显正价 |
| B、第一电离能可能Y小于X |
| C、气态氢化物的稳定性:HmY小于HnX |
| D、最高价含氧酸的酸性:X对应的酸性弱于于Y对应的 |
用NA表示阿伏加德罗常数,下列判断正确的是( )
| A、常温常压下,16g O2和O3的混合气体中含有NA个氧原子 |
| B、常温常压下,28 g CO与22.4 L O2的分子数都是NA个 |
| C、16 g CH4与18 g NH4+所含质子数都是10NA个 |
| D、1 mol/L Na2CO3溶液中,CO32-的离子数目小于NA个 |
下列实验设计能完成或实验结论合理的是( )
| A、证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾--淀粉试纸检验,观察试纸颜色的变化 |
| B、铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,铝热剂中一定不含铁的氧化物 |
| C、将SO2通入Ba(NO3)2溶液,有白色沉淀生成,证明BaSO3难溶于硝酸 |
| D、在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 |