题目内容
19.下列说法正确的是( )| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 天然气、太阳能、生物质能、风能、氢能均属于新能源 | |
| C. | 自发反应的熵一定增大,非自发反应的熵一定减小 | |
| D. | 常温下,反应C(s)+CO2(g)?2CO(g)不能自发进行,则该反应的△H>0 |
分析 A、不能根据反应条件来判断反应吸放热;
B、天然气为化石能源;
C、反应自发与否,决定于熵变和焓变两个因素;
D、反应C(s)+CO2(g)?2CO(g)为熵增的反应.
解答 解:A、不能根据反应条件来判断反应吸放热,反应吸放热与反应条件无必然关系,即需要加热的反应不一定是吸热反应,故A错误;
B、天然气为化石能源,属于传统能源,不是新能源,故B错误;
C、反应自发与否,决定于熵变和焓变两个因素,焓变和熵变共同决定反应是否自发,不能只根据熵变来判断反应能否自发,故C错误;
D、反应C(s)+CO2(g)?2CO(g)为熵增的反应,故若为非自发,则反应一定吸热,故D正确.
故选D.
点评 本题考查了反应自发与否的条件,△H-T△S>0反应不能自发进行,反之,反应能够自发进行,以及焓变与反应条件无关.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.1918年,德国化学家弗里茨•哈伯因为发明合成氨方法而获得诺贝尔化学奖.1931年,卡尔•博施因为改进合成氨方法获得诺贝尔化学奖.2007年10月诺贝尔化学奖授予了德国化学家格哈德•埃特尔,理由是他发现了哈伯一博施法合成氨的作用机理.现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生,下列有关说法正确的是( )
| A. | 达到化学平衡时,将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| D. | 达到化学平衡时,正反应速率和逆反应速率都为零 |
7.浓硝酸不具有的性质是( )
| A. | 不稳定性 | B. | 可溶解水晶 | C. | 强氧化性 | D. | 易挥发性 |
14.下列实验方法:
①用蒸馏法分离C2H5OH与C6H5-OH(沸点为182℃)的混合物
②用盐析法分离油脂皂化反应的产物
③用升华法分离I2和砂子的混合物
④用重结晶法分离KNO3和NaCl的混合物
⑤用分液法分离H2O和C2H5-Br的混合物.
你认为上述方法( )
①用蒸馏法分离C2H5OH与C6H5-OH(沸点为182℃)的混合物
②用盐析法分离油脂皂化反应的产物
③用升华法分离I2和砂子的混合物
④用重结晶法分离KNO3和NaCl的混合物
⑤用分液法分离H2O和C2H5-Br的混合物.
你认为上述方法( )
| A. | 只有①不正确 | B. | ②⑤不正确 | C. | 只有③④正确 | D. | 全部正确 |
8.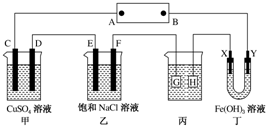 如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )
 如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色.则以下说法正确的是( )| A. | 电源B极是正极 | |
| B. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:1 | |
| C. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷 |
9.下列实验设计方案错误的是( )
| A. | 除去Cu(NO3)2溶液中混有的AgNO3:加入适量铜粉 | |
| B. | 分离溴和CCl4的混合物:分液 | |
| C. | 区分NaCl和KCl溶液:焰色反应 | |
| D. | 检验某未知溶液中的SO42-:加入稀硝酸酸化的BaCl2溶液 |
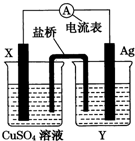 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池,如图所示.请回答下列问题.