题目内容
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1
(1)生产中为提高反应速率和SO2的转化率,下列措施可行的是
A.向装置中充入N2 B.向装置中充入过量的SO2C.向装置中充入O2 D.升高温度
(2)若在一定温度下,向一个容积可变的恒压容器中,通入3mol SO2 和2mol O2及固体催化剂,发生上述反应,平衡时容器内气体体积为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5mol O2(g)、1mol SO3 (g),下列说法正确的是
A.第一次平衡时反应放出的热量为294.9kJ
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等
D.第二次平衡时SO3的体积分数等于
(3)生产中在550℃时,将2.0mol SO2和1.0mol O2置于5L密闭容器中,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图1所示.反应达平衡后,体系总压强为0.10M Pa.试计算反应2SO3?2SO2+O2 在550℃时的平衡常数K= .A、B表示不同压强下的平衡转化率,通常工业生产中采用常压的原因是: ,并比较不同压强下的平衡常数:K(0.10MPa) K(1.0MPa)(填“<”或“>”或“=”).
(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl-=[AgCl2]-,如图2是某温度下AgCl在NaCl溶液中的溶解情况.由以上信息可知:
①由图知该温度下AgCl的溶度积常数为 .
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是: .
(1)生产中为提高反应速率和SO2的转化率,下列措施可行的是
A.向装置中充入N2 B.向装置中充入过量的SO2C.向装置中充入O2 D.升高温度
(2)若在一定温度下,向一个容积可变的恒压容器中,通入3mol SO2 和2mol O2及固体催化剂,发生上述反应,平衡时容器内气体体积为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5mol O2(g)、1mol SO3 (g),下列说法正确的是
A.第一次平衡时反应放出的热量为294.9kJ
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等
D.第二次平衡时SO3的体积分数等于
| 2 |
| 9 |
(3)生产中在550℃时,将2.0mol SO2和1.0mol O2置于5L密闭容器中,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如图1所示.反应达平衡后,体系总压强为0.10M Pa.试计算反应2SO3?2SO2+O2 在550℃时的平衡常数K=
(4)沉淀物并非绝对不溶,且在水及各种不同的溶液中溶解度有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变.已知AgCl+Cl-=[AgCl2]-,如图2是某温度下AgCl在NaCl溶液中的溶解情况.由以上信息可知:
①由图知该温度下AgCl的溶度积常数为
②AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:

考点:化学平衡的调控作用,化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:(1)该反应是一个反应前后气体体积减小的放热反应,欲提高SO2的转化率,则改变条件使平衡向正反应方向移动;
(2)A、根据体积之比等于物质的量之比计算平衡时混合气体总的物质的量,再利用差量法计算参加反应的二氧化硫的物质的量,结合热化学方程式计算放出的热量;
B、恒温恒压,两次达到平衡状态相同分析计算判断;
C、恒温恒压,两次达到平衡状态相同分析判断
D、根据A计算可知,原平衡时SO3的体积分数为
=
;
(3)根据化学平衡计算的三段式进行计算,压强之比等于物质的量之比,依据平衡常数概念计算;
压强的增加引起SO2转化率的变化并不明显,所以工业上直接采用常压,平衡常数随温度变化;
(4)①由AgCl的溶度积Ksp(AgCl)=c(Ag+)?c(Cl-)计算;
②开始Cl-抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl-浓度增大使AgCl形成[AgCl2]-络合物,所以Ag+浓度又变大了.
(2)A、根据体积之比等于物质的量之比计算平衡时混合气体总的物质的量,再利用差量法计算参加反应的二氧化硫的物质的量,结合热化学方程式计算放出的热量;
B、恒温恒压,两次达到平衡状态相同分析计算判断;
C、恒温恒压,两次达到平衡状态相同分析判断
D、根据A计算可知,原平衡时SO3的体积分数为
| 1mol |
| 4.5mol |
| 2 |
| 9 |
(3)根据化学平衡计算的三段式进行计算,压强之比等于物质的量之比,依据平衡常数概念计算;
压强的增加引起SO2转化率的变化并不明显,所以工业上直接采用常压,平衡常数随温度变化;
(4)①由AgCl的溶度积Ksp(AgCl)=c(Ag+)?c(Cl-)计算;
②开始Cl-抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl-浓度增大使AgCl形成[AgCl2]-络合物,所以Ag+浓度又变大了.
解答:
解:(1)A、向装置中充入N2,化学平衡不会移动,不会提高二氧化硫转化率,故A错误;
B、向装置中充入过量的SO2,二氧化硫转化率降低,故B错误;
C、向装置中充入过量的O2,化学平衡正向移动,会提高二氧化硫转化率,故C正确;
D、升高温度,化学平衡逆向移动,二氧化硫的转化率减小,故D错误.
故选:C;
(2)A、由题意气体体积为起使时的90%,则反应后总的物质的量为起始时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×
=98.3KJ,故A错误;
B、2SO2+O2?2SO3
起始量(mol) 3 2 0
变化量(mol) x 0.5x x
平衡量(mol)3-x 2-0.5x x
反应后总的物质的量为起始时的90%,3-x+2-0.5x+x=4.5,x=1mol,二氧化硫转化率=
×100%=
;
保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5mol O2(g)、1mol SO3(g),转化为起始量为6molSO2(g)、4molO2,恒压条件下两次平衡时等效平衡,平衡后二氧化硫应为4mol,转化率=
×100%=20%,故B错误;
C、依据B分析可知等效平衡状态,氧气体积分数相同,故C正确;
D、原平衡时SO3的体积分数为
=
,故D正确;
故答案为:CD;
(3)体系总压强为0.10M Pa,此时二氧化硫的转化率为80%
2SO2+O2
2SO3
起始量(mol) 2 1 0
变化量 (mol)2×0.8 0.8 2×0.8
平衡量 (mol) 0.4 0.2 1.6
平衡时各物质的浓度为:c(SO2)=0.08mol/L,c(O2)=0.04mol/L,c(SO3)=0.32mol/L 代入平衡常数的计算式得到
平衡常数K=
=
=400,
则反应2SO3?2SO2+O2 在550℃时的平衡常数K=
=2.5×10-3;
从图象中可以看出,常压SO2就可以达到较高的转化率,压强的增加引起SO2转化率的变化并不明显,加压必须增大投资以解决增加设备和提供能量问题,所以工业上直接采用常压,平衡常数随温度变化,不随压强变化,平衡常数不变;
故答案为:2.5×10-3;常压下400~500°C,SO2转化率已经很高了,加压必须增大投资以解决增加设备和提供能量问题;=;
(4)①当c(Ag+)=10-5mol/L时,c(Cl-)=10-7mol/L,所以AgCl的溶度积常数Ksp=c(Ag+)?c(Cl-)=10-5mol/L×10-7mol/L=10-12(mol/L)2,
故答案为:10-12;
②开始Cl-抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl-浓度增大使AgCl形成[AgCl2]-络合物:AgCl+Cl-=[AgCl2]-,所以Ag+浓度又变大了,
故答案为:开始Cl-抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl-浓度增大使AgCl形成[AgCl2]-络合物,所以Ag+浓度又变大了.
B、向装置中充入过量的SO2,二氧化硫转化率降低,故B错误;
C、向装置中充入过量的O2,化学平衡正向移动,会提高二氧化硫转化率,故C正确;
D、升高温度,化学平衡逆向移动,二氧化硫的转化率减小,故D错误.
故选:C;
(2)A、由题意气体体积为起使时的90%,则反应后总的物质的量为起始时的90%,平衡时总物质的量为(3mol+2mol)×90%=4.5mol,则平衡时各组成物质的量变化为:
2SO2+O2?2SO3物质的量减少△n
2 1 2 1
1mol 0.5mol 1mol (3mol+2mol)-4.5mol=0.5mol
此时放出的热量为196.6KJ×
| 0.5mol |
| 1mol |
B、2SO2+O2?2SO3
起始量(mol) 3 2 0
变化量(mol) x 0.5x x
平衡量(mol)3-x 2-0.5x x
反应后总的物质的量为起始时的90%,3-x+2-0.5x+x=4.5,x=1mol,二氧化硫转化率=
| 1mol |
| 3mol |
| 1 |
| 3 |
保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5mol O2(g)、1mol SO3(g),转化为起始量为6molSO2(g)、4molO2,恒压条件下两次平衡时等效平衡,平衡后二氧化硫应为4mol,转化率=
| 1mol |
| 5mol |
C、依据B分析可知等效平衡状态,氧气体积分数相同,故C正确;
D、原平衡时SO3的体积分数为
| 1mol |
| 4.5mol |
| 2 |
| 9 |
故答案为:CD;
(3)体系总压强为0.10M Pa,此时二氧化硫的转化率为80%
2SO2+O2
| 催化剂 |
| △ |
起始量(mol) 2 1 0
变化量 (mol)2×0.8 0.8 2×0.8
平衡量 (mol) 0.4 0.2 1.6
平衡时各物质的浓度为:c(SO2)=0.08mol/L,c(O2)=0.04mol/L,c(SO3)=0.32mol/L 代入平衡常数的计算式得到
平衡常数K=
| c2(SO3) |
| c2(SO2)?c(O2) |
| 0.322 |
| 0.082×0.04 |
则反应2SO3?2SO2+O2 在550℃时的平衡常数K=
| 1 |
| 400 |
从图象中可以看出,常压SO2就可以达到较高的转化率,压强的增加引起SO2转化率的变化并不明显,加压必须增大投资以解决增加设备和提供能量问题,所以工业上直接采用常压,平衡常数随温度变化,不随压强变化,平衡常数不变;
故答案为:2.5×10-3;常压下400~500°C,SO2转化率已经很高了,加压必须增大投资以解决增加设备和提供能量问题;=;
(4)①当c(Ag+)=10-5mol/L时,c(Cl-)=10-7mol/L,所以AgCl的溶度积常数Ksp=c(Ag+)?c(Cl-)=10-5mol/L×10-7mol/L=10-12(mol/L)2,
故答案为:10-12;
②开始Cl-抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl-浓度增大使AgCl形成[AgCl2]-络合物:AgCl+Cl-=[AgCl2]-,所以Ag+浓度又变大了,
故答案为:开始Cl-抑制了AgCl的溶解,所以Ag+浓度变小了,但Cl-浓度增大使AgCl形成[AgCl2]-络合物,所以Ag+浓度又变大了.
点评:本题考查了平衡影响因素,平衡计算分析,注意平衡建立和反应条件选择的方法和依据及平衡常数计算应用,沉淀溶解平衡以图象分析为基础,题目难度较大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
油脂的硬化属于( )反应.
| A、氧化 | B、加成 | C、取代 | D、化合 |
在一定条件下,下列物质可与甲烷发生化学反应的是( )
| A、溴水 | B、氯水 |
| C、氧气 | D、高锰酸钾溶液 |
在一定条件下的密闭容器中,进行反应:I2(g)+H2(g)?2HI(g),下列有关说法不正确的是( )
| A、达到平衡时,正反应速率等于逆反应速率 |
| B、增大氢气的浓度可增大反应速率 |
| C、在上述条件下,氢气能全部转化为碘化氢 |
| D、达到平衡时,体系中各物质的质量分数不再改变 |
2013年3月,黄浦江上游水质污染较为严重,相关自来水厂采用多种方法并用的方式进行水质处理,下列说法中错误的是( )
| A、加活性炭可吸附水中小颗粒,净化水质的方法属于物理方法 |
| B、用聚合硫酸铁作为净水剂,该处理过程中仅发生了化学变化 |
| C、用细菌与酶的扩充法去除水中的氨氮的方法属于生物法 |
| D、加臭氧对水进行消毒,利用了臭氧的氧化性 |
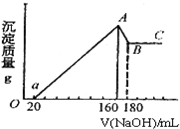 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.