题目内容
11.1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)?bZ(g).反应达到平衡后,测得X的转化率为25%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的$\frac{5}{6}$,则a和b数值可能是( )| A. | a=1,b=2 | B. | a=1,b=3 | C. | a=2,b=3 | D. | a=2,b=1 |
分析 反应达到平衡后,测得X的转化率为25%,则转化的X为1mol×25%=0.25mol,则
X(g)+aY(g)?bZ(g)
开始 1 a 0
转化 0.25 0.25a 0.25b
平衡 0.75 0.75a 0.25b
在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的$\frac{5}{6}$,则$\frac{\frac{m}{1+a}}{\frac{m}{0.75+0.75a+0.25b}}$=$\frac{5}{6}$,以此来解答.
解答 解:反应达到平衡后,测得X的转化率为25%,则转化的X为1mol×25%=0.25mol,则
X(g)+aY(g)?bZ(g)
开始 1 a 0
转化 0.25 0.25a 0.25b
平衡 0.75 0.75a 0.25b
在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的$\frac{5}{6}$,则$\frac{\frac{m}{1+a}}{\frac{m}{0.75+0.75a+0.25b}}$=$\frac{5}{6}$,解得1+a=3b,
A.a=1,b=2时,1+a<3b,故A不选;
B.a=1,b=3时,1+a<3b,故B不选;
C.a=2,b=3时,1+a<3b,故C不选;
D..a=2,b=1时,1+a=3b,故D选;
故选D.
点评 本题考查化学平衡的计算,为高频考点,把握平衡三段法、a与b的关系为解答的关键,侧重分析与计算能力的考查,该题还可定性分析气体体积减小来解答,题目难度不大.

| A. | Na2O | B. | Na2O2 | C. | MgCl2 | D. | H2S |
| A. | 苯 | B. | 乙醇 | C. | 乙烯 | D. | 二氧化硫 |
| A. | 向纯水中加入少量固体碳酸钠,c(H+)减小,Kw不变,促进水的电离 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,变小 | |
| C. | 将纯水加热到95℃时,变大,pH不变,水仍呈中性 | |
| D. | 向水中加入A1C13固体,平衡正向移动,c(OH-)增大 |
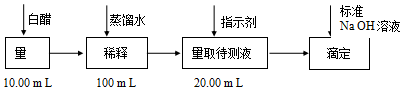
完成下列填空:
(1)稀释白醋时需要的仪器有烧杯、玻璃棒、胶头滴管、100mL容量瓶.
(2)应选用酚酞作为指示剂.达到滴定终点时,指示剂从无色变为浅红色.
(3)某同学一共进行了三次实验.以下是他设计的实验数据记录表,表格中A是滴定前读数,B是滴定后读数.
| 实验次数 | 稀释后白醋 体积(mL) | 标准NaOH溶液 | ||
| A | B | 消耗体积(mL) | ||
| 1 | 20.00 | 22.05 | ||
| 2 | 20.00 | 21.34 | ||
| 3 | 20.00 | 21.30 | ||
若测得稀释后白醋的浓度0.0594mol/L,则该食醋符合(选填“符合”、“不符合”)国家标准.
标准NaOH溶液通过以下步骤准备:①配制500mL浓度约为0.1mol/L的NaOH溶液;
②用KHC8H4O4标准溶液准确测定该NaOH溶液的浓度.
(4)称量所需的NaOH固体置于大烧杯中,加入500mL蒸馏水,搅拌溶解,该配制步骤可行可行
(填“可行”或“不可行”).
(5)NaOH标准溶液的浓度需通过测定而不能直接配制的原因是NaOH固体在称量时容易吸收空气中的水和CO2,使配制所得的溶液浓度低于预期浓度,导致实验误差.
| A. | 无水硫酸铜粉末遇水变蓝色 | |
| B. | 氢氧化铁胶体使水中悬浮物聚沉 | |
| C. | 盛在无色试剂瓶中的浓硝酸呈黄色 | |
| D. | FeSO4溶液久置于空气中,溶液呈黄色 |
| A. | 实验②证明了①的滤液中含有Ag+,由此推断①的滤液中也含有Cl- | |
| B. | 实验②证明了Kap(AgCl)<Kap(Ag2SO4) | |
| C. | 实验③的溶液中含有+微粒 | |
| D. | 由实验③推测:若在①的沉淀中滴加NaOH溶液,沉淀也能溶解 |
