题目内容
2.分析发现,某陨石中含有半衰期极短的铝的一种同位素2713Al,该同位素的原子核内的中子数是( )| A. | 12 | B. | 14 | C. | 16 | D. | 18 |
分析 原子中:质子数是13,质量数是27,中子数=质量数-质子数,据此分析.
解答 解:2713Al中质子数是13,质量数是27,中子数=质量数-质子数=27-13=14,
故选B.
点评 本题考查了质子数、中子数和质量数的关系,难度不大,明确质量数和中子数、质子数之间的关系是解本题的关键.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
13.下列有关化学平衡和速率的说法正确的是( )
| A. | H2、I2、HI平衡混合气体加压后颜色不变 | |
| B. | 恒温恒压的密闭体系中进行的合成氨反应,达到平衡后,充入惰性气体,氨气的体积分数增大 | |
| C. | 红棕色的NO2气体加压后,颜色先变深,后变浅 | |
| D. | 任意温度下都能自发的反应一定是放热和熵减的反应 |
17.已知热化学方程式:
Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-351.5kJ•mol-1;
Hg(l)+$\frac{1}{2}$O2(g)═HgO(s)△H=-90.84kJ•mol-1,
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)═ZnO(s)+Hg(l)的△H为( )
Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-351.5kJ•mol-1;
Hg(l)+$\frac{1}{2}$O2(g)═HgO(s)△H=-90.84kJ•mol-1,
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)═ZnO(s)+Hg(l)的△H为( )
| A. | △H=+260.66 kJ•mol-1 | B. | △H=-260.66 kJ•mol-1 | ||
| C. | △H=-442.34 kJ•mol-1 | D. | △H=+442.34 kJ•mol-1 |
14.下列事实中,能说明苯环与侧链的相互影响会导致苯酚的化学性质与苯或醇不同的是( )
| A. | 1mol苯酚与3mol H2发生加成反应 | B. | 苯酚能和NaOH溶液反应 | ||
| C. | 苯酚燃烧产生带浓烟的火焰 | D. | 苯酚与浓溴水反应生成三溴苯酚 |
11.下列物质中,不能发生水解反应的是( )
| A. | 油脂 | B. | 淀粉 | C. | 蔗糖 | D. | 葡萄糖 |
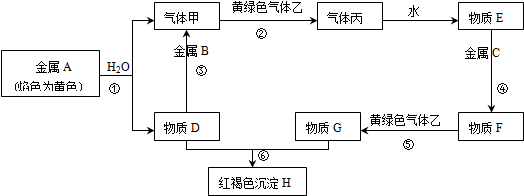
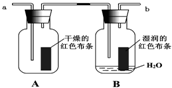 为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答:
为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答: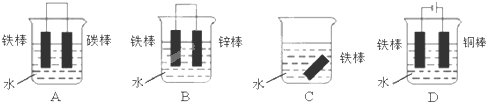
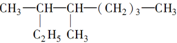 的名称是3,4一二甲基辛烷
的名称是3,4一二甲基辛烷 ,1mol该烃完全燃烧需消耗氧气18.5mol.
,1mol该烃完全燃烧需消耗氧气18.5mol.