题目内容
11.下列关于热化学的说法正确的是( )| A. | 需要加热才能发生的反应是吸热反应 | |
| B. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出热量少 | |
| C. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 | |
| D. | 由热化学方程式 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
分析 A、某些放热反应也需要加热才能发生;
B、等质量的硫蒸汽和硫固体,前者的能量高;
C、化学反应的反应热取决于反应物和生成物的能量的差值;
D、合成氨的反应为可逆反应,不能进行彻底.
解答 解:A、某些放热反应也需要加热才能发生,故需要加热才能发生的反应不一定是吸热反应,也可能是放热反应,故A错误;
B、等质量的硫蒸汽和硫固体,前者的能量高,故当完全燃烧生成二氧化硫时,放出的热量前者多,故B错误;
C、化学反应的反应热取决于反应物和生成物的能量的差值,即取决于始态和终态,与反应路径无关,故C正确;
D、合成氨的反应为可逆反应,不能进行彻底,故1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,释放出的热量小于92kJ,故D错误.
故选C.
点评 本题考查热化学方程式的含义和反应热的大小判断,题目难度不大,做题时要注意热化学方程式中反应热与物质的物质的量成正比,取决于始态和终态,与反应路径无关.

练习册系列答案
相关题目
2.下列说法正确的是( )
| A. | 化学反应速率通常用单位时间内反应物或生成物的质量变化来表示 | |
| B. | 化学反应速率的单位由浓度单位决定 | |
| C. | 在反应过程中,反应物的浓度逐渐变小,所以用反应物表示的化学反应速率为负值 | |
| D. | 用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 |
19.下列关于离子化合物的叙述正确的是( )
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 离子化合物一定可以导电 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
6. W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第VIA族;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是Cl->N3->O2->Na+(用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、Cl2、ClO2 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是H2S(填化学式),沸点高的是H2O(填化学式)
(6)ZW的电子式为Na+[:H]-,W2Y2的电子式为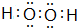 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: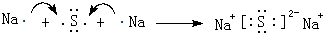 .
.
(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液不褪色(填“褪色”或“不褪色”),请用相关离子方程式解释原因SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
(8)已知
工业制镁时,电解MgCl2而不电解MgO的原因是氧化镁熔点高,耗能多;制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融时不导电.
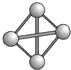
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N入出942kJ.根据以上信息和数据,下列说法正确的是C.
A.N4属于一种新型化合物
B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2
D.1molN4转变为N2将吸收882KJ的能量.
 W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第VIA族;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是Cl->N3->O2->Na+(用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、Cl2、ClO2 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是H2S(填化学式),沸点高的是H2O(填化学式)
(6)ZW的电子式为Na+[:H]-,W2Y2的电子式为
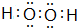 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: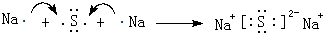 .
.(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液不褪色(填“褪色”或“不褪色”),请用相关离子方程式解释原因SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
(8)已知
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N入出942kJ.根据以上信息和数据,下列说法正确的是C.
A.N4属于一种新型化合物
B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2
D.1molN4转变为N2将吸收882KJ的能量.
16.取浓度相同的NaOH和HCl溶液,以2:3体积比相混合,所得溶液的pH等于1,则原溶液的浓度为( )
| A. | 0.01 mol•L-1 | B. | 0.017 mol•L-1 | C. | 0.05 mol•L-1 | D. | 0.50 mol•L-1 |
1.下列A、B两种元素,其中可以组成AB2型离子化合物的是( )
| A. | C和O | B. | Na和S | C. | Mg和Cl | D. | Ne和O |