题目内容
元素性质随着原子序数的递增呈现周期性变化的根本原因的是( )
| A、原子核外电子排布呈周期性变化 |
| B、元素的相对原子质量逐渐增大 |
| C、原子半径呈现从大到小的周期性变化 |
| D、元素化合价呈周期性变化 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:根据随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化来解答.
解答:
解:A、因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故A正确;
B、因随原子的相对原子质量的递增,元素发生变化,但不能说明周期性变化,故B错误;
C、因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故C错误;
D、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故D错误;
故选:A.
B、因随原子的相对原子质量的递增,元素发生变化,但不能说明周期性变化,故B错误;
C、因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故C错误;
D、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故D错误;
故选:A.
点评:本题考查元素周期律的实质,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,并注意不能用元素本身的性质来解释元素性质的周期性变化.

练习册系列答案
相关题目
下列溶液一定呈中性的是( )
| A、pH=7的溶液 |
| B、c(H+)=c(OH-)的溶液 |
| C、非电解质溶于水得到的溶液 |
| D、由强酸、强碱等物质的量反应得到的溶液 |
下列说法中不正确的是( )
| A、羧基是乙酸的官能团,羟基是乙醇的官能团 |
| B、乙酸与碳酸钠反应生成二氧化碳气体,说明乙酸的酸性强于碳酸 |
| C、乙酸和乙醇反应生成乙酸乙酯的反应属于酸碱中和反应 |
| D、乙酸乙酯是密度比水小的、无色透明的、不溶于水的、有香味的油状液体 |
相等物质的量的CO和CO2相比较,下列有关叙述不正确的是( )
| A、它们所含的电子数目之比为1:1 |
| B、它们所含的O原子数目之比为1:2 |
| C、它们所含的C原子数目之比为1:1 |
| D、它们所含的原子总数目之比为2:3 |
下列条件的变化对醋酸的电离常数产生影响的是( )
| A、增大醋酸的浓度 |
| B、向溶液中加水 |
| C、增大压强 |
| D、升高温度 |
下列反应:8NH3+3Cl2═6NH4Cl+N2,氧化剂和还原剂的质量比是( )
| A、8:3 |
| B、213:136 |
| C、34:213 |
| D、213:34 |
下列各组物质能在水溶液中大量共存的是( )
| A、Na+、K+、HCO3-、CO32- |
| B、Ca2+、Ba2+、HCO3-、OH- |
| C、Na+、HSO4-、S2-、SO32- |
| D、Ca2+、Na+、HCO3-、ClO- |
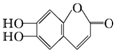 中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是
中药狼把草的成分之一M具有消炎杀菌作用,M的结构如图所示:下列叙述正确的是( )
| A、M的相对分子质量是180 |
| B、M与足量的NaOH溶液发生反应消耗2molNaOH |
| C、1mol M与足量NaHCO3反应生成2mol CO2 |
| D、1mol M最多能与3mol Br2发生反应 |